Grup hemo
Un grup hemo és un grup prostètic que forma part de diverses proteïnes, com per exemple l'hemoglobina dels eritròcits de la sang dels vertebrats, dels quals és el pigment responsable del color vermell. Tenen una estructura formada per anells que envolten un àtom de ferro, que es pot enllaçar feblement a l'oxigen molecular (O₂), al diòxid de carboni (CO₂) i a altres petites molècules.[1]


Als pulmons l'hemoglobina s'uneix feblement amb oxigen i forma oxihemoglobina; a través de la vena pulmonar i el sistema arterial, la sang transporta l'oxihemoglobina fins al conjunt de les cèl·lules del cos, on es dissocia altra vegada en hemoglobina i oxigen, cosa que els farà possible la respiració. I després la mateixa hemoglobina s'associa al diòxid de carboni provinent del metabolisme cel·lular per formar la carbaminohemoglobina o carbohemoglobina, que a través del sistema venós i l'artèria pulmonar farà cap als pulmons, on es dissociarà en hemoglobina i diòxid de carboni, que s'expulsarà a l'exterior.[2]
Estructura química modifica
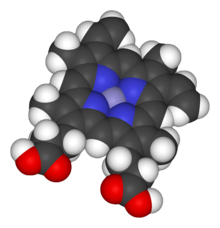
Els grups hemo estan formats per quatre anells de pirrole (protoporfirina IX), formant un tetrapirrole cíclic que conté al seu centre un catió ferro(2+) en una estructura molecular plana. Aquest ió forma quatre enllaços amb els respectius nitrògens de cada cadena polipèptica de pirrole, un cinquè enllaç coordinat amb un nitrogen d'una histidina, perpendicular cap amunt, i un sisè enllaç feble perpendicular cap avall, què és on es capta i allibera l'oxigen gas (O₂) que l'hemo transporta amb ell. L'estructura que envolta el ferro evita dins del cos humà que aquest s'oxidi formant un Fe3+ que no deixaria anar l'oxigen captat.[3] Alguns agents oxidants poden provocar que s'oxidi, impedint així que la sang pugui transportar oxigen. Això pot ocórrer per una ingestió o inhalació de certs tòxics[4] o, per exemple, en fer-nos un tall a la sang que surt fora. En aquesta sang l'hemoglobina s'oxida formant metalhemoglobina a causa de l'oxigen de l'aire.[5]
La seva estructura és força similar a la d'un altre pigment, la clorofil·la, que conté un àtom de magnesi en comptes d'un de ferro, cosa que fa que el pigment resultant sigui verd en comptes de vermell.[2] La fotosíntesi es basa en la clorofil·la mentre que la respiració dels vertebrats es basa en els grups hemo -en té quatre- de l'hemoglobina.[6]
Característiques modifica
En principi l'hemo té propietats apolars, però té també un extrem polar amb càrrega negativa. És hidròfob i insoluble en aigua. L'oxigen tampoc no és gaire soluble en aigua, és per això que, per exemple, al cos humà, la quantitat d'oxigen transportat pel grup hemo present a l'hemoglobina de la sang és setanta vegades superior a l'oxigen que es transporta directament al plasma sanguini.[3]
Tipus modifica
Es poden destacar tres grups hemo per la seva importància biològica: l'hemo a, l'hemo b i l'hemo c.
- L'hemo a no té cap enllaç covalent amb l'apoproteïna a la qual es troba i es caracteritza per contenir una cadena lateral amb un metil que es pot oxidar formant un aldehid i una cadena lateral vinil. N'és un exemple l'enzim citocrom c oxidasa.
- L'hemo b és molt semblant a l'hemo a: tampoc no forma enllaç covalent amb la proteïna a la qual es troba i es diferencia de la a en el fet que no té el grup metil i que en lloc del vinil té una cadena isoprenoïde. És el tipus d'hemo més habitual, present per exemple a l'hemoglobina, la mioglobina i la neuroglobina
- L'hemo c té la mateixa estructura que el b, però amb la diferència que l'hemo c si forma enllaços covalents amb la proteïna a la qual es troba, i en forma dos, precisament a cada una de les dues cadenes vinil. Exemples de proteïnes que contenen grups hemo de tipus c són el citocrom c i el complex citocrom bc1.
Tòxics i contaminants modifica
La introducció de metalls pesants (per exemple el plom) dins del cos dels humans i altres animals vertebrats, per exemple a través de la respiració, pot atacar la síntesi i el funcionament dels seus grups hemo, a més d'altres processos metabòlics. Per exemple, se sap que a partir de vint micres de plom per decilitre de sang aquest interfereix a la síntesi del grup hemo, cosa que pot produir una anèmia.[7]
Referències modifica
- ↑ Anàlisi química quantitativa, de Daniel Harris. Editorial Reverte, 2006. ISBN 9788429172232 (català)
- ↑ 2,0 2,1 Conceptes de termodinàmica química i cinètica, d'Enric Brillas. Edicions Universitat de Barcelona, 2004. ISBN 9788447528424 (català)
- ↑ 3,0 3,1 Fonaments de bioquímica, de Juli Garcia Peretó, Universitat de València, 2005. ISBN 9788437062686 (català)
- ↑ Tòxics, verins, drogues i contaminants, Universitat Autònoma de Barcelona, 2008. ISBN 9788449025518 (català)
- ↑ Recull d'experiments de Química, Edicions Universitat de Barcelona, 2011. ISBN 9788447534791 (català)
- ↑ Geologia i química del cosmos i de la Terra, de Josep Maria Amigó. Universitat de València, 2002. ISBN 9788437052649 (català)
- ↑ El canvi global vist per un químic preocupat, de Fernando Sapiña. Universitat de València, 2001. ISBN 9788476606308 (català)