Virus de la febre aftosa del bestiar
El virus de la febre aftosa del bestiar (en anglès Foot-and-mouth disease virus o FMDV) és l'agent causal de la febre aftosa del bestiar. Es tracta del membre prototip del gènere Aphtovirus, dins de la família Picornaviridae. La glossopeda (del grec, γλώσσος glossos, llengua i πεδη peda, pota, peülla) o febre aftosa del bestiar (FMD) és una malaltia infecciosa aguda que afecta els membres de l'ordre Artiodactyla, que inclou el bestiar boví, oví, caprí i porcí a més d'altres animals salvatges.[1] La FMD es caracteritza per febres altes durant dos o tres dies i l'aparició d'úlceres a la boca i llengua, anomenades aftes, a més d'ampolles a les peülles i al braguer. L'alta contagiositat del virus i les pèrdues en la producció associades fan que la febre aftosa del bèstiar sigui una preocupació en la sanitat animal arreu del món.
| Foot-and-mouth disease virus | |
|---|---|
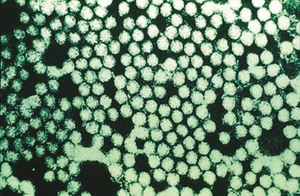 Microfotografia electrònica del virus de la febre aftosa del bestiar | |
| Dades | |
| Genoma | Grup IV ((+)ssRNA) |
| Malaltia | glossopeda |
| Taxonomia | |
| Regne | Orthornavirae |
| Fílum | Pisuviricota |
| Classe | Pisoniviricetes |
| Ordre | Picornavirales |
| Família | Picornaviridae |
| Gènere | Aphthovirus |
| Espècie | Foot-and-mouth disease virus |
| Nomenclatura | |
| Sinònims | Glossopeda
|
Història modifica
La primera descripció escrita de la febre aftosa probablement es va fer el 1514, quan Fracastorius descriu una malaltia similar en bestiar a Itàlia. Gairebé 400 anys després, el 1897, Loeffler i Frosch van demostrar per primera vegada que una malaltia dels animals, la febre aftosa en qüestió, era causada per un agent filtrable. No va ser fins a l'any 1920 que un model animal adequat va ser establert per Waldmann i Pape per a l'estudi del virus de la febre aftosa, utilitzant conillets d'índies, i amb el posterior desenvolupament de sistemes de cultiu in vitro de cèl·lules pel virus, les propietats químiques i físiques del virus de la febre aftosa es van anar descobrint durant la resta del segle xx, arribant el 1989 a una descripció completa de la seva estructura tridimensional.[2]
Etiologia de la FMD modifica
L'agent causal de la glossopeda és el virus de la febre aftosa del bestiar, pertanyent al gènere Aphtovirus, dins de la famíilia Picornaviridae.
Estructura del virus modifica
Es tracta d'un virus ARN monocatenari el genoma del qual es troba inclòs en una càpside proteica, sense embolcall. La seva mida està al voltant dels 30 nm i la càpside té morfologia icosaèdrica amb pentàmers formats per 4 proteïnes estructurals diferents: VP1, VP2, VP3 i VP4. D'aquestes, la proteïna VP1 és la més important, ja que constitueix un dels antígens més immunògens i biològicament actius del virus, en intervenir en el reconeixement dels receptors cel·lulars i la formació d'anticossos neutralitzants. Aquesta proteïna és, a més, altament variable, el que la fa responsable en bona part de l'elevada variabilitat del virus. El genoma víric està format per uns 8500 nucleòtids i s'estructura en una fase de lectura oberta (ORF) central situada entre dues zones no codificadores. La zona no codificadora situada a l'extrem 5' té unida covalentment la proteïna VPg.
Serotips modifica
S'han identificat 7serotips i uns 65 subtipus del virus de la febre aftosa. Per ordre d'identificació, van ser designats O (Oise) i A (Allemagne) el 1922, C el 1926; SAT1, SAT2, SAT3 (territoris sud-africans) entre 1952-1958 i Asia1 el 1957. Les tècniques d'hibridació d'ARN permeten dividir els tipus en dos grups diferents: O, A, C i Asia 1 i SAT,1,2 i 3, amb una homologia del 60 al 10% dins de cada grup i de només 25-40% entre grups. Tradicionalment cada tipus ha estat dividit al seu torn en subtipus basant-se en diferències quantitatives mitjançant tècniques serològiques i de protecció creuada. En cada tipus té lloc una variació antigènica que correspon a un procés continu de deriva antigènica per mutacions puntuals sense existir límits de separació clars entre subtipus. Aquesta heterogeneïtat antigènica té importants implicacions econòmiques en el desenvolupament i selecció de vacunes, ja que la immunitat adquirida mitjançant infecció o vacunació és estrictament específica de tipus, i en menor mesura, específica de subtipus.[3]
Variabilitat modifica
A la gran varietat de serotips i subtipus s'hi afegeix el fet que el virus de la febre aftosa és extremadament variable des del punt de vista genòmic, mostrant gran facilitat per modificar les seqüències que codifiquen tant les seves proteïnes estructurals com les no estructurals i també per fer estables les noves variacions.
S'han descrit mecanismes similars als que presenten els virus influença, com el “drift” antigènic, un canvi menor caracteritzat per una certa quantitat de reemplaçaments aminoacídics. Però també s'han descrit altres canvis de gran magnitud en què certs aminoàcids de localització crítica es veuen substituïts, alterant d'aquesta manera diversos epítops o determinants antigènics alhora (l'anomenat “shift” antigènic en virus influença). Es poden arribar a donar variacions antigèniques en el curs d'una mateixa ona epizoòtica. Aquesta variabilitat no només es restringeix a elements estructurals o funcionals, sinó que poden determinar una marcada modificació de les propietats biològiques, com la virulència del virus enfront diverses espècies animals.
Característiques físico-químiques modifica
El virus queda inactivat ràpidament fora de l'interval de pH de 6,0-9,0 i per dessecació i temperatures superiors als 56 °C, tot i que el virus residual pot sobreviure un temps considerable quan s'associa amb proteïnes d'origen animal (per exemple en llet infectada i pasteuritzada a 72 °C durant 15 seg). El virus és resistent a dissolvents lipídics com l'èter i cloroform però a causa de la seva sensibilitat a pHs alcalins i àcids, l'hidròxid de sodi, el carbonat de sodi, i l'àcid cítric o l'àcid acètic són desinfectants eficaços.[4]
Replicació viral modifica
Quan el virus entra en contacte amb la membrana d'una cèl·lula hoste, s'uneix a un lloc receptor, provoca un plegament de la membrana i la travessa.
Després de l'adsorció, penetració i eliminació de la càpside del virió, la VPg, que és una petita proteïna que s'uneix covalentment a l'extrem 5’ de les cadenes del RNA + i RNA - i al RNA del virió però no a l'ARNm, se separa del de l'ARN víric mitjançant l'acció dels enzims cel·lulars.
L'ARN víric, actuant com ARNm, és traduït sense interrupcions per donar una poliproteïna amb activitat proteasa. Aquesta és dividida posteriorment en quatre productes primaris que, al seu torn, són dividits de nou en proteïnes més petites per subunitats o parts de la pròpia poliproteïna amb activitat proteassa. Els primers passos d'aquesta escissió tenen lloc quan la poliproteïna encara està unida al polirribosoma.
Un dels polipèptids resultants de la fragmentació primària dona lloc, després de la seva divisió, a quatre proteïnes estructurals i un altre producte primari és el precursor de la part vírica de l'ARN polimerasa. La funció dels altres dos polipèptids primaris és desconeguda. Aquestes proteïnes estructurals del virus estan codificades a l'extrem 5’, mentre que les altres proteïnes virals que intervenen en la replicació viral, patogènia i processament proteolític, són codificades cap a l'extrem 3’.[5]
La replicació de l'ARN víric es dona al citoplasma. L'ARN polimerasa transcriu una cadena complementària (sentit negatiu) que serveix al seu torn com a motlle per a la síntesi de noves cadenes de sentit positiu. Aquestes cadenes de sentit positiu actuen llavors com ARNm addicional per a la posterior síntesis de proteïnes virals o bé són incorporades en els virions de la progènie.
El cicle infecciós es completa amb l'empaquetament del genoma del virus a la càpside i la sortida d'aquesta de la cèl·lula infectada.
El virus de la febre aftosa, i en general els picornavirus, posseeixen la característica de poder dur a terme la recombinació intramolecular dels seus genomes quan la cèl·lula està doblement infectada per dues soques diferents de la mateixa espècie vírica, fet que s'ha demostrat tant en el cas del virus de la febre aftosa com en el del poliovirus[6]
Resposta immunològica modifica
Immunitat innata modifica
El virus de la febre aftosa (VFA), quan infecta un animal, és percebut per cèl·lules de la immunitat innata, com ara els macròfags. Quan hi ha reconeixement dels patrons moleculars del virus per part d'aquestes cèl·lules, es produeixen gran varietat de citocines proinflamatories com el factor de necrosi tumoral alfa (TNF-a) i l'INF1 i es fagocita el virus. S'ha demostrat que la fagocitosi del VFA pels macròfags és possible sense l'ajuda dels anticossos opsonitzants, encara que l'activitat fagocítica d'aquestes cèl·lules es torna molt més eficient quan intervé el sistema complement.[7]
En contrast amb això, els experiments basats en cultius cel·lulars han demostrat que és necessari que el VFA estigui unit per un anticòs específic amb la finalitat d'induir la transcripció d'IFN de les cèl·lules dendrítiques. Això implicaria un important alliberament d'INF de les cèl·lules drendrítiques en resposta a la infecció per aquest virus, però això no es produirà fins que la concentració d'anticossos anti-VFA en la circulació hagi aconseguit nivells adequats.[8]
Els mecanismes pels quals el VFA interacciona amb les cèl·lules el sistema immunitari innat requereixen més recerca.
Immunitat específica modifica
La producció d'anticossos comença amb la IgM, seguida de IgG, que aviat constitueix la immunoglobulina majoritària i capaç de neutralitzar al virus. La producció d'anticossos enfront del virus es duu a terme per limfòcits B, com ocorre en altres animals. Aquests limfòcits, per produir els anticossos necessiten, d'una banda, reconèixer alguna regió del virus i per un altre rebre un senyal d'activació dels limfòcits T helpers. Aquests limfòcits T han hagut de ser activats prèviament reconeixent pèptids de les proteïnes del virus en la membrana de cèl·lules presentadores d'antigen i associat a molècules del sistema major d'histocompatibilitat o MHC.
Aquests alts nivells d'anticossos es troben en el sèrum d'animals que han patit la malaltia o que han estat vacunats i poden ser detectats en la circulació dels animals infectats 4-5 dies després de la infecció natural.[9]
Evasió modifica
A més d'una supressió general de la síntesi de proteïnes de les cèl·lules hoste, el virus de la febre aftosa ha desenvolupat diversos mecanismes per a l'evasió efectiva de la resposta immunitària de l'hoste com ara la interferència específica per la inhibició de la síntesi de IFN. El VFA també és capaç d'interferir amb l'expressió superficial de les molècules de MHC de classe I.
Els limfòcits T citotòxics CD8+ s'activen per destruir les cèl·lules infectades pel virus després de la detecció dels pèptids vírics presentats per les molècules de MHC de classe I. En impedir l'expressió de la superfície de l'antigen viral, el virus de la febre aftosa és capaç d'eludir aquesta branca específica de la resposta immunitària cel·lular.
No obstant això també s'ha demostrat que la repressió de les molècules de MHC de classe I poden desencadenar la citotoxicitat de les cèl·lules NK, i per tant poden intervenir l'eliminació de les cèl·lules infectades pel virus a través d'aquest mecanisme.[7]
Malalties produïdes pel virus modifica
Els aftovirus infecten a una àmplia gamma d'espècies animals domèstiques i salvatges de peülla enfonsada (artiodàctils). El cavall és refractari a la infecció; les vaques, el búfal d'aigua, les ovelles, les cabres, les llames, els camells i els porcs, en canvi, són susceptibles i presenten signes clínics. A més dels animals domèstics, són susceptibles a la infecció natural o experimental més de 70 espècies d'animals salvatges pertanyents a més de 20 famílies.
L'aparició d'un brot de febre aftosa en una explotació afecta generalment a totes les espècies susceptibles, però a vegades el virus s'adapta sobretot a una espècie. En general, els signes clínics són més greus en el bestiar boví i porcí, però s'han descrit brots en porcs mentre que les vaques en contacte estret amb ells no desenvolupaven la malaltia. Les ovelles i les cabres solen presentar infeccions subclíniques. Els animals salvatges mostren una gamma de respostes que va des de la infecció inaparent a la malaltia greu i, fins i tot, la mort
Febre aftosa en bòvids modifica
Després d'un període d'incubació que pot durar de 2 a 8 dies, apareix febre, pèrdua de gana, depressió i una notable disminució de la producció de llet. Després de 24 hores, comença un baveig continu de saliva i apareixen vesícules sobre la llengua i les genives. L'animal, a vegades, pot obrir i tancar la boca amb un típic so "d'espetec agut". També poden observar-se vesícules a la pell de l'espai interdigital i al cantell coronari de les peülles i sobre els mugrons.
Les vesícules es trenquen ràpidament donant lloc a grans lesions ulceratives desprotegides. Les localitzades a la llengua solen curar-se en pocs dies, però les situades en les peülles i dins la cavitat nasal amb freqüència resulten infectades per bacteris, donant lloc a coixeres i flux nasal mucopurulent que es perllonguen un llarg temps.
En els vedells de fins a 6 mesos d'edat, el virus de la febre aftosa pot produir miocarditis que condueixen a la mort (sol ser ràpida i no arriben a mostrar les vesícules i els altres signes clínics que apareixen en els adults). La mortalitat en els animals adults és molt escassa però, tot i que el virus no travessa la placenta, les vaques poden avortar en conseqüència a les febres. A més, els animals infectats presenten una producció baixa o nul·la durant períodes llargs. Aquesta baixada de producció ve donada per la desaparició de la gana, les intenses coixeres, les mastitis i els avortaments.
Febre aftosa en suids modifica
En el bestiar porcí, les coixeres solen ser el primer signe. Les lesions podals poden ser greus i suficientment doloroses per impedir que els animals romanguin drets. Les zones desprotegides situades entre les peülles solen resultar infectades per bacteris i, en conseqüència, es produeix supuració i a vegades la caiguda del teixit corni i l'aparició de coixeres perllongades.
Les vesícules de l'interior de la boca solen ser menys importants que en el bestiar boví, tot i que és freqüent l'existència de grans vesícules que es trenquen ràpidament a la zona del musell.
Febre aftosa en altres animals modifica
La malaltia clínica en ovelles, cabres i remugants salvatges sol ser més benigna que en el bestiar boví i es caracteritza per la presentació de lesions podals acompanyades de coixeres.[5]
Febre aftosa en humans modifica
La febre aftosa és una malaltia vírica que afecta freqüentment al bestiar i que, a vegades, pot afectar a l'ésser humà. S'han descrit només uns 40 casos de febre aftosa en humans, la majoria presenten com a font d'infecció accidents de laboratori i infecció deguda a munyir vaques infectades. Són pocs els casos de transmissió per ingesta de llet crua, carn fresca, poc cuita, fumada i curada. Entre les manifestacions clíniques s'inclouen febre, cefalea, postració, dolors musculars, vesícules i úlceres a tota la mucosa oral.[7]
Patogènia modifica
Els animals susceptibles poden ser infectats pel virus de la febre aftosa a conseqüència del contacte directe o indirecte amb animals infectats o amb elements contaminats, el període d'incubació oscil·la entre els 2 i 14 dies.
Després de la incubació té lloc la infecció de les cèl·lules de l'àrea orofaríngia on es replica i dissemina a les zones adjacents a través del torrent circulatori i limfàtic. Un cop arriba als nòduls limfàtics infecta les ubicacions de preferència fins a desenvolupar lesions.
A continuació, el virus es presenta en altes concentracions en secrecions com fluids nasals, bucals, femtes, orina, llet, mucus vaginal, semen... Comencen a aparèixer les vesícules a la cavitat oral, nasal, potes i esporàdicament al rumen, salivació, descàrrega nasal i coixeres.
Després d'un curt període les vesícules es trenquen formant úlceres i evolucionen els signes clínics, finalitza la febre i la virèmia per a començar la producció d'anticossos detectables. En aquest període s'inicia la cicatrització de les lesions, l'animal torna a alimentar-se i disminueixen els títols del virus en els fluids i teixits. Tot i que la cicatrització s'ha completat, el virus roman a la regió orofaríngia donant lloc a un individu portador.[7]
Epidemiologia modifica
Els virus del gènere Aphtovirus produeixen una única malaltia, la febre aftosa o glossopeda, que constitueix un greu problema a tot el món. En moment o altre, la malaltia ha aparegut a la major part del món, normalment causant extenses epidèmies en vaques, ovelles i porcs. A més són susceptibles molts animals silvestres.
La mortalitat d'aquest procés és baixa però la morbilitat és molt alta, la convalescència dels animals afectats és perllongada i provoca que la febre aftosa sigui tan important, especialment quan apareix en països prèviament lliures de malaltia.
La febre aftosa és la malaltia vírica més important que limita l'eficàcia de la producció animal en moltes zones del món, per aquest motiu la seva epidemiologia s'ha estudiat profundament. Presenta una epidemiologia molt complexa deguda a diversos factors:
- La malaltia existeix de manera enzoòtica en els quatre continents.
- Abundància de diferents tipus de virus.
- Àmplia gamma d'espècies animals domèstiques i salvatges poden resultar infectades de manera natural.
- Diversitat de mecanismes i rapidesa en la disseminació.
- Desenvolupament d'infeccions persistents en algunes espècies.
Països lliures de la febre aftosa enzoòtica modifica
En els països en els quals la malaltia no ha aparegut o ha estat erradicada, pot desenvolupar-s'hi ràpidament una epizoòtia fructífera conseqüència de la introducció de la malaltia en una sola explotació. En un breu lapse de temps, freqüentment dies, el brot pot estendre’s de tal manera que les autoritats veterinàries tinguin problemes per controlar-ne la difusió. Això és degut a l'elevada naturalesa infecciosa del virus causant, inclosa la producció d'aerosols de virus per part dels animals infectats i el curt període d'incubació.
La febre aftosa s'estén ràpidament en una zona mitjançant el moviment d'animals infectats al mercat i, a vegades, mitjançant transmissió mecànica del virus a animals susceptibles per part de fòmits (roba, sabates i eines veterinàries). L'excreció del virus pot ser fins a 24 hores abans que apareguin els primers signes clínics, això indica que la disseminació del virus entre explotacions ha pogut tenir lloc abans que se sospités la presència de la malaltia.
Una característica molt important que potencia la transmissió i l'aparició d'epidèmies és la possibilitat de difusió aèria. Aquest tipus de difusió depèn de la direcció i la velocitat del vent i es veu afavorida pels factors que redueixen la taxa d'inactivació del virus (baixes temperatures, humitat elevada i cels coberts). Tenint en compte aquests factors és lògic que la transmissió aèria a llarga distància sigui més freqüent en climes temperats que en tropicals.
El moviment d'animals de producció entre països està molt controlat, per aquest motiu la majoria d'aparicions del virus de la febre aftosa en països no endèmics es considera resultat de l'alimentació de porcs amb residus carnis infectats o conseqüència de la difusió a llarga distància d'aerosols vírics. Per tal de determinar l'origen d'infeccions entre països s'utilitzen tècniques d'identificació dels oligonucleòtids del RNA víric i dels polipèptids.
Països enzoòtics modifica
Les epizoòties poden ser causades per la introducció d'un tipus víric no present prèviament en un país, ja que el bestiar no tindrà en aquell moment una immunitat adquirida a través de la infecció natural o vacunació.
Poden existir llargs períodes en els quals no es detecta la malaltia i, quan s'investiga una zona àmplia, es pot trobar només un petit nombre d'animals amb lesions de poca importància. Això s'explica de diverses maneres:
- En alguns països (sobretot amb clima temperat i amb races europees) la gravetat de la malaltia està alterada per l'efecte de la vacunació.
- En països subtropicals i tropicals (sobretot amb races bovines locals) podria semblar que el virus ha evolucionat amb l'hoste, de tal manera que les soques enzoòtiques només produeixen un procés benigne en les vaques autòctones però originen una malaltia greu en les races bovines introduïdes. En aquests països només s'aprecien completament els problemes econòmics quan es comença a millorar la producció bovina mitjançant la importació de vaques provinents d'altres països.
- En països en desenvolupament d'Àfrica i Àsia hi trobem tipus antigènics del virus de la febre aftosa de major complexitat que els d'Europa i Sud-amèrica. A l'Àfrica existeix una major població d'animals salvatges que poden intervenir en l'epidemiologia (el búfal africà (Syncerus caffer) sembla l'hoste natural per a la perpetuació dels tipus SAT 1, 2 i 3 del virus de la febre aftosa). No s'ha descrit la presència de malaltia clínica en búfals tot i que molts en són portadors i, a més, no sembla que transmeti la malaltia a les vaques domèstiques.
Durant el segle xix, la febre aftosa es va detectar a Europa, Àsia, Àfrica, Amèrica i, en una ocasió, a Austràlia.[6]
En la taula següent es mostra la distribució actual de la malaltia:
Detecció del virus de la febre aftosa modifica
En el camp de la immunologia, tradicionalment els mètodes emprats en la detecció i identificació del virus de la febre aftosa han estat els de tipus serològic, amb proves com la fixació del complement o la seroneutralització. Són proves amb limitacions: no permeten estudiar l'evolució del virus ni determinar l'origen dels focus, perquè els sèrums estudiats tindran composicions variades en funció dels epítops als quals hagin hagut de fer front, i aquest predomini d'un o altre tipus d'anticòs influirà en els resultats.
Actualment, en aquestes proves, s'utilitzen nous reactius que els confereixen una gran sensibilitat. Són reactius formats per anticossos monoclonals que reaccionaran davant d'un únic epítop de la partícula viral. Permeten establir “impressions antigèniques” a partir de les quals es podran diferenciar les soques virals entre elles i les vacunals.
Els mètodes bioquímics són de gran utilitat per estudiar acuradament l'estructura de les soques virals. Permeten detectar les diferències i determinar la identitat, l'especificitat i l'evolució dels virus. Aquests mètodes inclouen l'electroforesi en gel de poliacrilamida, l'electrofocalització de les proteïnes virals i la seqüenciació de l'àcid nucleic i els AA de la proteïna viral.
Quant a l'especificitat i la sensibilitat, els avantatges de les noves tècniques perfeccionades són evidents. Tot i això, s'hauran de tenir en compte altres aspectes com la velocitat d'execució i el cost per tal que realment esdevinguin mètodes pràctics per l'estudi d'aquest virus.
El mètode ELISA és ràpid i s'adapta bé al diagnòstic d'aquesta malaltia i a la serotipificació dels virus. És una prova molt específica en què, si es treballa amb anticossos monoclonals, s'assoleix una gran sensibilitat. Aquest mètode ofereix perspectiva per comparar virus en funció de les seves propietats immunògenes i poder preveure les característiques protectores de les soques vacunals davant de les soques aïllades al camp.[10]
Planificació de l'erradicació de la febre aftosa: ecosistemes i estratègies regionals modifica
Les mesures de control i prevenció s'han d'adequar a la situació epidemiològica del país i/o l'ecosistema en qüestió.
Determinació geogràfica i mesures a prendre modifica
1. Ecosistema endèmic o endèmic primari modifica
Els ecosistemes endèmics contenen tots els elements necessaris per al manteniment de la malaltia: l'agent, els individus susceptibles i el mecanisme de transmissió. Són sistemes que es caracteritzen per una transmissió lenta i continua del virus, generalment a nivell subclínic o si més no, sense que es pugui percebre els signes amb facilitat. Per aquest motiu els ecosistemes endèmics són absolutament prioritaris per a l'eliminació de la malaltia.
Quant a la lluita contra la malaltia, la primera mesura que s'ha de prendre consisteix a prevenir la sortida d'animals joves sensibles o infectats, implicats en l'aparició de focus de febre aftosa a les àrees d'engreix. S'aconsegueix amb períodes de quarantena i amb la revacunació dels animals destinats a la producció en altres explotacions. Aquesta operació es realitza a la propietat d'origen, de 5 a 7 dies abans del desplaçament i té com a objectiu evitar la dispersió del virus.
Per eliminar el virus endèmic, s'ha d'actuar sobre la resta del bestiar mitjançant un ampli espectre de vacunes d'alta qualitat, generalment amb adjuvant oliós perquè confereixen una immunitat més prolongada.
Finalment, per comprovar si les mesures adoptades han tingut l'efecte esperat es realitzaran enquestes anuals d'anticossos-VIA (anticossos contra antígens associats a la infecció viral). Se cercarà, sobretot, la reducció de la prevalença a la categoria d'animals de menys de 2 anys.
2. Ecosistema epiendèmic o endèmic secundari modifica
Els ecosistemes epiendèmics contenen tots els elements necessaris per al manteniment de la malaltia i, a més, es produeix un intercanvi d'individus susceptibles o fonts d'infecció (entrades) i d'immunes (sortides) de manera que augmenta el nombre de casos.
El progrés de la malaltia en aquestes regions depèn econòmicament i epidemiològica del flux de joves mascles de les regions anteriors. En aquest cas, doncs, la planificació de l'erradicació de la febre aftosa és secundària i es posa èmfasi en les mesures preventives, sent la vacunació el mètode més eficaç. En cas que aparegui un brot, per a reduir el risc de l'aparició d'un de secundari, s'apliquen àmplies quarantenes i es procedeix a la immobilització dels animals.
3. Ecosistema paraendèmic modifica
L'ecosistema manca dels elements necessaris per al manteniment de la malaltia. La malaltia apareix esporàdicament com a conseqüència de la combinació d'interaccions amb elements externs.
4. Ecosistema lliure del virus modifica
Tot i que no es considera una zoonosi i, per tant, les persones no han de veure’s afectades pel consum de carn d'un animal malalt, des d'un punt de vista econòmic i polític, un país exportador de carn es veurà molt beneficiat quan es declari exempt de malaltia.
En aquests dos últims ecosistemes les característiques de maneig del bestiar no afavoreixen els mecanismes epidemiològics que permeten el manteniment del virus, de manera que en cas que la malaltia s'introduís, s'autolimitaria.[10] L'accent en les mesures de control es posa en la disminució del cost privat de l'atenció sanitària animal. Si es pot posar en pràctica un control adequat de la circulació animal, es pot reduir fortament el nombre de vacunacions regulars. La vacunació única, juntament amb un sistema de control de la malaltia ben organitzat, permetria un control eficient dels possibles focus amb vacunacions en anell,[11] que són aquelles vacunacions que es practiquen a una zona determinada, al voltant d'un focus, per a tenir-lo sota control el més ràpid possible (vacunació d'emergència). Aquesta vacunació es completarà amb el sacrifici sanitari dels ramats infectats, l'eliminació dels seus cadàvers i la neteja i desinfecció de les explotacions.
Referències modifica
- ↑ The Center for Food Security & Public Health. (2007) "Foot and Mouth Disease." Iowa State University College of Veterinary Medicine
- ↑ Brian W. J. Mahy (2005). Introduction and history of foot-and-mouth disease virus. Curr Top Microbiol Immunol. 288:1-8.
- ↑ C. Carrillo, Z. Lu, M. V. Borca, A. Vagnozzi, G. F. Kutish and D. L. Rock (2007). Genetic and Phenotypic Variation of Foot-and-Mouth Disease Virus during Serial Passages in a Natural Host. Journal of Virology.
- ↑ Brian W. J. Mahy, et al. (2012). Overview of Foot-and-Mouth Disease. The Merck Veterinary Manual.
- ↑ 5,0 5,1 Gutierrez A.(1994). El virus de la fiebre aftosa. Bovis. 56, 31-40
- ↑ 6,0 6,1 Fenner F., Bachmann P.A, Gibbs E. P. J, Murphy F. A., Studdert M. J, White D. O. (1987). Veterinary virology. Londres: Accademic Press
- ↑ 7,0 7,1 7,2 7,3 Díaz. A. P, Bautista L. Fiebre aftosa:Revisión de una enfermedad de impacto bovino. Bogotá: Universidad Colegio Mayor de Cundinamarca. Vist 17 de gener de 2014 de: http://www.slideshare.net/laurislau1/fiebre-aftosa-20369126
- ↑ McCulloughand K., Sobrino S.(2004). Immunology of Foot-and-Mouth Disease [versió electrònica]. Foot-and-Mouth Disease. Vist 18 de gener de 2014 de: http://www.crcnetbase.com/doi/abs/10.1201/9781420037968.ch8[Enllaç no actiu]
- ↑ Rodríguez A. (1994). Respuesta inmune frente al virus de la fiebre aftosa. Bovis. 56, 41-47
- ↑ 10,0 10,1 Office internarional des epizooties, Febre aftosa: 17a. Conferència (1986)
- ↑ Vacunación contra la gripe aviar: documento de información de la OIE, de: http://www.oie.int/fileadmin/Home/esp/Animal_Health_in_the_World/docs/pdf/E_Guidelines_on_AI_vaccination.pdf