Carbur d'alumini
El carbur d'alumini, o tricarbur de tetraalumini, és un compost inorgànic format per cations alumini(3+), , i anions carbur, , de fórmula Es presenta en forma de pols o de sòlids cristal·lins que poden ser de color groc-marró o de color verd-marró.
 | |
| Substància química | tipus d'entitat química |
|---|---|
| Massa molecular | 143,92615452 Da |
| Estructura química | |
| Fórmula química | Al₄C₃ |
| SMILES canònic | |
| Identificador InChI | Model 3D |
| Propietat | |
| Punt de fusió | 2.100 °C |
| Cristal·lografia | |
| Sistema cristal·lí | sistema trigonal |
Propietats modifica
El carbur d'alumini presenta una densitat de 2,36 g/cm³ i el seu punt de fusió, és de 1 400 °C. Aquest compost es descompon quan es posa en contacte amb aigua calenta, així com per addició d'àcid clorhídric diluït i per addició d'àcid sulfúric concentrat. El producte de la descomposició en ambdós casos és el metà:[1]
Classificació modifica
El carbur d'alumini forma part dels carburs iònics, que son aquells que presenten un caràcter fort de sal i es formen sobretot a partir dels elements dels grups I i II de la taula periòdica. Els elements d'aquests grups són molt electropositius i el carboni en conseqüència presenta una càrrega positiva.
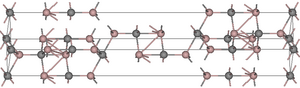
Estructura modifica
Presenta una estructura cristal·lina poc freqüent, que consta de dues capes de Al2C i Al2C2. Cada àtom d'alumini es troba en coordinació amb 4 carburs d'alumini per donar una estructura tetraèdrica. Existeixen dos àtoms de carboni en ambients d'unió diferents; per una banda un octaedre de 6 àtoms d'alumini a una distància de 217 pm. L'altre és una estructura en forma de bipiràmide trigonal distorsionada formada per 4 àtoms d'alumini a una distància de 190 a 194 pm i 5 àtoms d'alumini a una distància de 221 pm.
Obtenció modifica
El carbur d'alumini es prepara per reacció directe entre alumini i carboni en un forn d'arc elèctric a uns 1000 °C en absència d'oxigen i nitrogen a partir de la reacció següent:[1]
Una alternativa és fer reaccionar òxid d'alumini o fosfat d'alumini amb carboni, produeix monòxid de carboni. Les reaccions són:[2]
També por obtenir-se per reacció de l'alumini amb el monòxid de carboni a alta temperatura:
Aparició modifica
Podem trobar petites quantitats de carbur d'alumini com a impureses del carbur de calci.
A la fabricació electrolítica d'alumini, el carbur d'alumini es forma com a resultat de la corrosió dels elèctrodes de grafit.
En materials compostos per una matriu de metall sobre la base d'una matriu d'alumini reforçat amb carburs no metàl·lics o fibres de carboni, el carbur d'alumini es forma com a producte no desitjat. En el cas de la fibra de carboni, reacciona amb la matriu d'alumini a temperatures superiors a 500 °C. Es pot aconseguir una inhibició de la reacció química mitjançant un recobriment de borur de titani (per exemple).
Aplicacions modifica
La seva aplicació principal és la utilització d'aquest compost als laboratoris per a l'obtenció de metà.
També pot ser utilitzat com a catalitzador o bé com a agent secant i agent reductor. Té diverses aplicacions en el sector de la metal·lúrgia, ja que pot actuar com a abrasiu en eines de tall d'alta velocitat i té aproximadament la mateixa duresa que el topazi.
Referències modifica
- ↑ 1,0 1,1 Wade, K.; Banister, A. J.. The Chemistry of Aluminium, Gallium, Indium and Thallium: Comprehensive Inorganic Chemistry (en anglès). Elsevier, 2016-06-07. ISBN 9781483153223.
- ↑ Advanced Inorganic Chemistry Vol-1 (en anglès). Krishna Prakashan Media. ISBN 9788187224037.
Enllaços externs modifica
- «Enciclonet - Carburo de aluminio» (castellà) [Consulta: 30 desembre 2020]
- «Ecured - Carburo de aluminio» (castellà) [Consulta: 30 desembre 2020]
- «Hoja informativa de sustancias peligrosas - Carburo de aluminio (PDF)» (castellà) [Consulta: 30 desembre 2020]
- «Ayudamos a conocer: Aluminio carburo» (en castellà). Arxivat de l'original el 2 juny 2016. [Consulta: 30 desembre 2020].


