Estearat de magnesi
L'Estearat de magnesi és el compost químic amb la fórmula Mg(C
18H
35O
2)
2. És un sabó, format per sal que conté dos equivalents d'estearat (l’anió de l’àcid esteàric) i un catió de magnesi (Mg2 +). L'estearat de magnesi és una pols blanca i insoluble en aigua. Les seves aplicacions aprofiten la seva suavitat, insolubilitat en molts dissolvents i baixa toxicitat. S'utilitza com a agent desprenent i com a component o lubricant en la producció de productes farmacèutics i cosmètics.[1]
| Substància química | tipus d'entitat química |
|---|---|
| Massa molecular | 590,512 Da |
| Rol | metabòlit primari i excipient |
| Estructura química | |
| Fórmula química | C₃₆H₇₀MgO₄ |
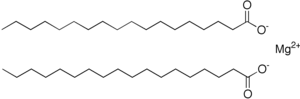 | |
| SMILES canònic | |
| Identificador InChI | Model 3D |
| NFPA 704: Standard System for the Identification of the Hazards of Materials for Emergency Response () | |
Producció
modificaL'estearat de magnesi es produeix per reacció de l'estearat de sodi amb sals de magnesi o mitjançant el tractament de l’òxid de magnesi amb àcid esteàric.[1] Alguns suplements nutricionals especifiquen que l'estearat de sodi utilitzat en la fabricació de l'estearat de magnesi es produeix a partir d'àcid esteàric d'origen vegetal.[2]
Usos
modificaL'estearat de magnesi s’utilitza sovint com a antiadherent[3] en la fabricació de comprimits, càpsules i pols mèdiques.[4] En aquest sentit, la substància també és útil perquè té propietats lubricants, evitant que els ingredients s’adhereixin als equips de fabricació durant la compressió de pols químics en pastilles sòlides; l'estearat de magnesi és el lubricant més utilitzat per a les pastilles.[5] No obstant això, pot causar una menor humectabilitat i una desintegració més lenta de les pastilles i una dissolució més lenta i fins i tot solubilitat del medicament.
L'estearat de magnesi també es pot utilitzar de manera eficient en processos de recobriment en sec.[6][7][8]
En la creació de caramels premsats, l'estearat de magnesi actua com a agent desprenent i s'utilitza per unir el sucre a caramels durs com els "mints".[9]
L'estearat de magnesi és un ingredient comú en les fórmules per a nadons.[10]
Curiositat
modificaL'estearat de magnesi és un component important dels cèrcols de brutícia que s'enganxen a la paret de la banyera. Quan són produïts per aigua i sabó, l'estearat de magnesi i l'estearat de calci formen un sòlid blanc insoluble en aigua i es coneixen col·lectivament com a escuma de sabó. En el cas dels cèrcols en aparells sanitaris, la sal esteàrica ha absorbit restes orgàniques provinents de la pell. La duresa de l'aigua en facilita la precipitació.[11]
Seguretat
modificaL'estearat de magnesi es considera generalment segur per al consum humà a nivells inferiors a 2.500 mg / kg al dia[12] i es classifica als Estats Units com a generalment reconegut com a segur (GRAS). El 1979, el subcomitè de la FDA sobre substàncies GRAS (SCOGS) va informar: "No hi ha proves a la informació disponible sobre ... estearat de magnesi ... que demostri, o suggereixi motius raonables per sospitar un perill per al públic quan és usat en nivells actuals i de la manera que es practica ara, o que es podria esperar raonablement en el futur."[13]
Referències
modifica- ↑ 1,0 1,1 Angelo Nora, Alfred Szczepanek, Gunther Koenen, "Metallic Soaps" in Ullmann's Encyclopedia of Industrial Chemistry 2005 Wiley-VCH, Weinheim. doi:10.1002/14356007.a16_361
- ↑ «Quick search results of the DSLD». National Institutes of Health. Arxivat de l'original el 29 d’octubre 2018.
- ↑ Ritter, Steve «What's That Stuff? Excipients: Inactive ingredients in medicines serve multiple functions in drug delivery». Chemical & Engineering News, 86, 1, 2008, pàg. 25. DOI: 10.1021/cen-v086n001.p025.
- ↑ Sworbrick, James; Boylan, James C. Encyclopedia of pharmaceutical technology, 1990, p. 2274. ISBN 9780824728243.
- ↑ Weiner, Myra L.; Kotkoskie, Lois A. Excipient Toxicity and Safety, 1999, p. 10. ISBN 9780824782108.
- ↑ Ouabbas Y, Dodds J., Galet L., Chamayou A., Baron M. «Particle-particle coating in a cyclomix impact mixer». Powder Technol., 189, 2, 2009, pàg. 245–252. DOI: 10.1016/j.powtec.2008.04.031.
- ↑ Thomas G., Ouabbas Y., Grosseau P., Baron M., Chamayou A., Galet L. «Modeling the main interaction forces between powder particles. Application to silica gel-magnesium stearate mixtures». Applied Surface Science, 255, 17, 2009, pàg. 7500–7507. Bibcode: 2009ApSS..255.7500T. DOI: 10.1016/j.apsusc.2009.03.099.
- ↑ Sato A., Serris E., Grosseau P., Thomas G., Galet L., Chamayou A., Baron M. «Experiment and simulation of dry particle coating». Chem. Eng. Science, 86, 2013, pàg. 164–172. DOI: 10.1016/j.ces.2012.07.037.
- ↑ https://www.ctahr.hawaii.edu/oc/freepubs/pdf/FST-9.pdf
- ↑ Erich Lück and Gert-Wolfhard von Rymon Lipinski. «Foods, 3. Food Additives». A: Ullmann's Encyclopedia of Industrial Chemistry. Weinheim: Wiley-VCH, 2002. DOI 10.1002/14356007.a11_561. ISBN 978-3527306732.
- ↑ Solos, Heather. «Cleaning The Bathtub» (en anglès). Home EC-101, 30-11-2009. [Consulta: 28 gener 2021].
- ↑ Søndergaarda, D.; Meyera, O.; Würtzena, G. «Magnesium stearate given peroprally to rats. A short term study». Toxicology, 17, 1, 1980, pàg. 51–55. DOI: 10.1016/0300-483X(80)90026-8. PMID: 7434368.
- ↑ FDA's SCOGS Database; Report No. 60; ID Code: 557-04-0; Year: 1979