Enllaç covalent coordinat
| Aquest article o secció no cita les fonts o necessita més referències per a la seva verificabilitat. |
S'anomena Enllaç covalent coordinat (en anglès dipolar bond) a l'enllaç químic que es forma quan dos cossos comparteixen un parell d'electrons, procedint aquests dos electrons d'un d'ells.
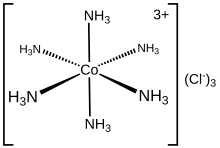
Aquest tipus d'enllaç es presenta quan un àtom no metàl·lic comparteix un parell d'electrons amb altres àtoms. Per tal que es doni aquest tipus d'enllaç, cal que l'àtom electro-positiu tingui un parell d'electrons lliures en un orbital exterior i que l'àtom electro-negatiu tingui capacitat per a rebre aquest parell d'electrons a la seva última capa de valència.
Aquest tipus d'enllaç és comú en els òxids no metàl·lics i en els ions complexos dels metalls lleugers, així com l'H₂SO₄, NH₃, SO₂. És també el responsable de certs ions com l'ió amoni (NH₄+), on el nitrogen cedeix els dos electrons perquè el quart hidrogen (que prèviament s'hauria ionitzat) s'uneixi a ell. És també important a l'ió oxoni (H₃O+), on l'oxigen cedeix el parell d'electrons.