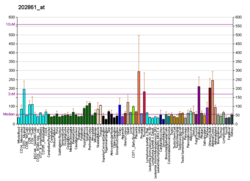
PER1
L'homòleg 1 de la proteïna circadiària del període és una proteïna en humans que està codificada pel gen PER1.[5]
El gen PER1 humà es troba al cromosoma 17 a la següent ubicació: [6]
- Inici: 8.140.470
- Finalització: 8.156.405
- Longitud: 15.936
- Exons: 24
PER1 té 19 transcripcions (variants d'empalmament).
Funció
modificaLa proteïna PER1 és important per al manteniment dels ritmes circadiaris a les cèl·lules i també pot tenir un paper en el desenvolupament del càncer. Aquest gen és un membre de la família de gens període. S'expressa amb un ritme circadiari oscil·lant diari, o una oscil·lació que fa un cicle amb un període d'aproximadament 24 hores. PER1 s'expressa sobretot a la regió del cervell anomenada nucli supraquiasmàtic (SCN), que és el marcapassos circadià primari del cervell dels mamífers. PER1 també s'expressa als teixits perifèrics dels mamífers.[7] Els gens d'aquesta família codifiquen components dels ritmes circadiaris de l'activitat locomotora, el metabolisme i el comportament. L'expressió circadiària de PER1 al nucli supraquiasmàtic s'executarà lliurement en la foscor constant, el que significa que el període de 24 hores del cicle persistirà sense l'ajuda de senyals de llum externa. Posteriorment, un canvi en el cicle llum/foscor evoca un canvi proporcional de l'expressió gènica al nucli supraquiasmàtic. El temps d'expressió gènica és sensible a la llum, ja que la llum durant la nit subjectiva d'un mamífer provoca un augment sobtat de per expressió i, per tant, un canvi de fase al nucli supraquiasmàtic.[8] S'ha observat splicing alternatiu en aquest gen; tanmateix, aquestes variants no s'han descrit completament. Hi ha cert desacord entre els experts sobre l'aparició de polimorfismes amb significació funcional. Molts científics afirmen que no hi ha polimorfismes coneguts del gen PER1 humà amb significació a nivell de població que doni lloc a canvis de comportament o fisiològics mesurables.[9] Tot i així, alguns creuen que fins i tot les mutacions silencioses poden causar fenotips de comportament significatius i donar lloc a canvis de fase importants.[10] La conservació funcional del gen PER es mostra en un estudi de Shigeyoshi et al. 2002. En aquest estudi, els gens mPer1 i mPer2 del ratolí van ser impulsats pel promotor atemporal de Drosophila a Drosophila melanogaster. Van trobar que ambdues construccions mPer podrien restaurar el ritme a les mosques arrítmiques (per01 mosques). Així, mPer1 i mPer2 poden funcionar com a components del rellotge en mosques i poden tenir implicacions pel que fa a l'homologia dels gens per.[11]
Paper en la cronobiologia
modificaEl gen PER1, també anomenat rigui, és un oscil·lador circadiari característic. PER1 es transcriu rítmicament al SCN, mantenint un període d'aproximadament 24 hores. Aquest ritme es manté en la foscor constant, i també es pot implicar en cicles de llum canviants.[12] PER1 participa en la generació de ritmes circadiaris al SCN, i també té un efecte en altres oscil·lacions a tot el cos. Per exemple, els knockouts de PER1 afecten els oscil·ladors d'aliments i els oscil·ladors circadiaris sensibles a la metamfetamina, els períodes dels quals es modifiquen en absència de PER1.[13] A més, els ratolins amb eliminacions tant en els gens PER1 com en PER2 no mostren ritme circadiari.[14] Els canvis de fase a les neurones PER1 es poden induir per un estímul de llum fort i breu al SCN de les rates. Aquesta exposició a la llum provoca augments de l'ARNm de PER1, cosa que suggereix que el gen PER1 té un paper important en l'entrenament del rellotge biològic dels mamífers al cicle llum-foscor.[15]
Mecanisme de retroalimentació
modificaL'ARNm PER1 s'expressa a totes les cèl·lules, actuant com a part d'un mecanisme de retroalimentació negativa de transcripció i traducció, que crea un rellotge molecular autònom de la cèl·lula. La transcripció de PER1 està regulada per interaccions de proteïnes amb els seus cinc elements E-box i un D-box a la seva regió promotora. L'heterodímer CLOCK - BMAL1 activa els elements de la caixa E presents al promotor PER1, a més d'activar els promotors de la caixa E d'altres components del rellotge molecular com PER2, CRY1 i CRY2. La fase d'expressió de l'ARNm de PER1 varia entre els teixits,[16] La transcripció surt del nucli i es tradueix a una proteïna amb dominis PAS, que permeten les interaccions proteïna-proteïna. PER1 i PER2 són fosforilats per CK1ε, la qual cosa condueix a una major ubiquitilació i degradació.[17] Aquesta fosforilació es contraresta amb la fosfatasa PP1, donant lloc a un augment més gradual del PER fosforilat i un control addicional sobre el període del rellotge molecular.[18] La fosforilació de PER1 també pot conduir a emmascarar la seva seqüència de localització nuclear rica en leucina i, per tant, impedir la importació d'heterodímers.[19]
Descobriment
modificaL'ortòleg PER1 va ser descobert per primera vegada per Ronald Konopka i Seymour Benzer el 1971. Durant l'any 1997 es van descobrir els gens del període 1 (mPer1) i del període 2 (mPer2) (Sun et al., 1997 i Albretch et al., 1997). Mitjançant pantalles d'homologia amb la Drosophila per, es van descobrir aquests gens. Va ser descobert de manera independent per Sun et al. 1997, anomenant-lo RIGUI i per Tei et al. 1997, que la va anomenar hper per la similitud de la seqüència de proteïnes amb Drosophila per. Van trobar que l'homòleg del ratolí tenia les propietats d'un regulador circadiari. Tenia expressió circadiària al nucli supraquiasmàtic (SCN), oscil·lació autosostenida i arrastre de l'expressió circadiària per senyals de llum externa.[20]
Referències
modifica- ↑ 1,0 1,1 1,2 GRCh38: Ensembl release 89: ENSG00000179094 - Ensembl, May 2017
- ↑ 2,0 2,1 2,2 GRCm38: Ensembl release 89: ENSMUSG00000020893 – Ensembl, May 2017
- ↑ «Human PubMed Reference:». National Center for Biotechnology Information, U.S. National Library of Medicine.
- ↑ «Mouse PubMed Reference:». National Center for Biotechnology Information, U.S. National Library of Medicine.
- ↑ Cell, 90, 6, 9-1997, pàg. 1003–11. DOI: 10.1016/S0092-8674(00)80366-9. PMID: 9323128 [Consulta: lliure].
- ↑ «PER1» (en anglès). NCBI. [Consulta: 18 gener 2015].
- ↑ Sleep Med., 8, 6, 9-2007, pàg. 547–56. DOI: 10.1016/j.sleep.2006.11.002. PMID: 17395534.
- ↑ Prog. Neurobiol., 50, 2–3, 10-1996, pàg. 109–32. DOI: 10.1016/S0301-0082(96)00032-9. PMID: 8971980.
- ↑ Ann. Neurol., 72, 3, 9-2012, pàg. 324–34. DOI: 10.1002/ana.23636. PMC: 3464954. PMID: 23034908.
- ↑ J. Hum. Genet., 51, 12, 2006, pàg. 1122–25. DOI: 10.1007/s10038-006-0060-y. PMID: 17051316 [Consulta: free].
- ↑ Genes Cells, 7, 2, 2-2002, pàg. 163–71. DOI: 10.1046/j.1356-9597.2001.00503.x. PMID: 11895480.
- ↑ Cell, 90, 6, 9-1997, pàg. 1003–11. DOI: 10.1016/S0092-8674(00)80366-9. PMID: 9323128 [Consulta: lliure].
- ↑ Proc. Natl. Acad. Sci. U.S.A., 109, 35, 8-2012, pàg. 14218–23. Bibcode: 2012PNAS..10914218P. DOI: 10.1073/pnas.1206213109. PMC: 3435193. PMID: 22891330 [Consulta: lliure].
- ↑ Cell, 105, 5, 6-2001, pàg. 683–94. DOI: 10.1016/S0092-8674(01)00380-4. PMID: 11389837 [Consulta: lliure].
- ↑ Neurosci. Lett., 294, 1, 11-2000, pàg. 41–44. DOI: 10.1016/S0304-3940(00)01545-7. PMID: 11044582.
- ↑ Nucleic Acids Res., 38, 22, 12-2010, pàg. 7964–73. DOI: 10.1093/nar/gkq678. PMC: 3001056. PMID: 20693532.
- ↑ NeuroReport, 11, 5, 4-2000, pàg. 951–55. DOI: 10.1097/00001756-200004070-00011. PMID: 10790862.
- ↑ Proc. Natl. Acad. Sci. U.S.A., 108, 39, 9-2011, pàg. 16451–56. Bibcode: 2011PNAS..10816451L. DOI: 10.1073/pnas.1107178108. PMC: 3182690. PMID: 21930935 [Consulta: lliure].
- ↑ J. Biol. Chem., 276, 49, 12-2001, pàg. 45921–27. DOI: 10.1074/jbc.M107726200. PMC: 1513547. PMID: 11591712 [Consulta: lliure].
- ↑ Cell, 91, 7, 12-1997, pàg. 1055–64. DOI: 10.1016/S0092-8674(00)80495-X. PMID: 9428527 [Consulta: lliure].