Ribosoma
Els ribosomes són orgànuls no membranosos només són visibles al microscopi electrònic a causa de la seva reduïda grandària (30 nm en cèl·lula procariota i 33 nm en eucariota). Es troben a totes les cèl·lules vives. Els ribosomes reuneixen la proteïna suficient per arreglar els defectes de la cèl·lula.[1]
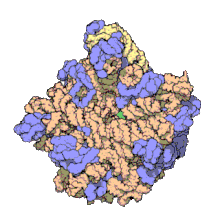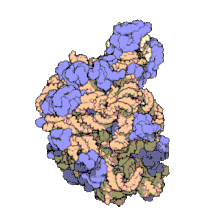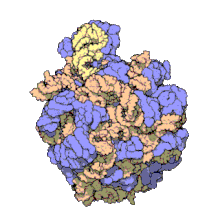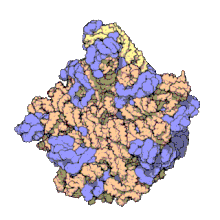
Un dels principis centrals de la biologia, al qual sovint es refereixen com el dogma central de la biologia molecular, és que l'ADN és utilitzat per fabricar ARN, que al seu torn s'utilitza per formar proteïnes. La seqüència genètica d'ADN és copiada en una molècula d'ARN missatger (ARNm). Després els ribosomes llegeixen la informació d'aquest ARNm i la utilitzen per crear proteïnes. Aquest procés en què els ribosomes utilitzen la informació genètica continguda en l'ARNm per formar proteïnes s'anomena traducció genètica. Ho fan enllaçant-se a una molècula d'ARNm i usant-la com una plantilla per determinar la seqüència correcta d'aminoàcids d'una proteïna concreta. Els aminoàcids estan units a una molècula d'ARN de transferència (ARNt), que entren a una part del ribosoma i s'uneixen a la seqüència d'ARNm. Els aminoàcids adjuntats són enllaçats llavors per una altra part del ribosoma. Els ribosomes es mouen seguint l'ARNm, llegint la seqüència de nucleòtids i produint una cadena amb la seqüència corresponent d'aminoàcids.
Els ribosomes estan fets de complexos d'ARN i proteïnes anomenades ribonucleoproteïnes. Es divideixen en dues subunitats. La més petita s'uneix a l'ARNm, mentre que la subunitat gran s'uneix al ARNt i als aminoàcids. Quan un ribosoma acaba de llegir una molècula d'ARNm, aquestes dues subunitats se separen. Els ribosomes es classifiquen com ribozims, ja que l'ARN ribosomal que els forma sembla el més important per l'activitat peptidil transferasa que uneix els aminoàcids entre si.
Els ribosomes dels bacteris, arqueans i eucariotes (els tres dominis de la vida a la Terra) tenen estructures i seqüències d'ARN molt diferents. Aquestes diferències estructurals permeten la utilització d'alguns antibiòtics per matar bacteris mitjançant la inhibició dels seus ribosomes, mentre que els ribosomes humans no queden afectats. Els ribosomes dels mitocondris i dels cloroplasts de les cèl·lules eucariotes s'assemblen en molts aspectes als dels bacteris, la qual cosa posa de manifest el probable origen evolutiu bacterià dels mitocondris i dels cloroplasts.[2][3] La paraula ribosoma prové d'àcid ribonucleic i de la paraula grega soma (que significa cos).
Altres Ribosomes
modificaA les cèl·lules eucariotes, als arqueans i als bacteris, els ribosomes es diferencien per la seva mida, composició i proporció de proteïnes per ARN. Com que estan formats per dues subunitats de diferent mida, els ribosomes són lleugerament més llargs a la part de l'eix que en la del diàmetre. Els ribosomes procariòtics tenen una mida al voltant de 20nm (200 Armstrongs) de diàmetre i estan formats per un 65% d'ARN ribosòmic i un 35% de proteïnes ribosòmiques. Els ribosomes eucariòtics tenen una mida que oscil·la entre 25 i 30nm (250-230 Armstrongs) de diàmetre i la proporció d'ARN ribosòmic per la de les proteïnes és propera a 1. Els ribosomes tradueixen l'ARN missatger (ARNm) i construeixen cadenes polipeptídiques (per exemple les proteïnes) utilitzant aminoàcids gràcies a l'ARN de transferència (ARNt).
Els ribosomes fabriquen proteïnes a partir de les instruccions genètiques que hi ha a la molècula d'ARN missatger. Els ribosomes lliures es troben en el citosol; altres es troben units al reticle endoplasmàtic rugós, la qual cosa li confereix una rugositat (d'aquí el perquè del seu nom), o a la coberta nuclear. Com que els ribozims[4] estan parcialment constituïts d'ARN, es pensa que podrien ser considerats com vestigis del món de l'ARN.[5] Són considerats com orgànuls, però l'ús d'aquest terme queda força restringit per a descriure components subcel·lulars que inclouen una membrana fosfolipídica que els ribosomes no tenen. Per aquest motiu, els ribosomes poden ser descrits com "orgànuls no membranosos".
Aquests orgànuls van ser observats com partícules o grànuls densos[6] per primer cop a mitjans de 1950 pel científic George Palade utilitzant un microscopi electrònic. Aquest fet el va portar a guanyar el Premi Nobel. El terme "ribosoma" va ser proposat pel científic Richard B. Roberts el 1958:
"Durant el curs del simposi, una dificultat semàntica es va fer evident. Per alguns participants, el terme "microsomes" fa referència a les partícules ribonucleoproteiques de la fracció dels microsomes contaminada per altres proteïnes i material lipídic; per d'altres, els microsomes estan constituïts de proteïnes i lípids contaminats per altres tipus de molècules. L'expressió "partícules microsomals" no sembla adequada, i "partícules ribonucleoproteiques de la fracció contaminada dels microsomes” és poc apropiada. Durant la reunió, la paraula "ribosoma" va ser proposada, la qual té un nom molt satisfactori i un so agradable. La confusió present seria eliminada si el terme "ribosoma" fos adaptat per a designar partícules ribonucleoproteiques de mida limitada entre 35 i 100s."
— Roberts, R. B., Microsomal Particles and Protein Synthesis[7]
L'estructura i la funció dels ribosomes i les molècules associades, complex conegut com a aparell translacional, ha estat d'interès de recerca des de mitjans del segle vint i és un àmbit molt actiu d'estudi avui en dia.
Els ribosomes estan compostos per dues subunitats que s'acoblen juntes i treballen com una sola estructura per a traduir l'ARNm en una cadena polipeptídica durant la síntesi de proteïnes. Les subunitats bacterianes consisteixen en una o dues molècules i les eucariòtiques d'una o tres molècules molt llargues d'ARN (conegut com a ARN ribosòmic o ARNr) i multitud de proteïnes més petites. El treball cristal·logràfic ha mostrat que no hi ha proteïnes ribosomals properes al lloc de reacció de la síntesi petídica. Això suggereix que els components proteics dels ribosomes actuen com una mena de bastida per millorar l'habilitat de l'ARNr per sintetitzar proteïnes més que per participar directament en la catàlisi.
Biogènesi
modificaA les cèl·lules bacterianes, els ribosomes són sintetitzats en el citoplasma a través de la transcripció de múltiples operons de gens ribosòmics. A les eucariotes el procés té lloc tant al citoplasma cel·lular com en el nuclèol, una regió del nucli cel·lular. El procés d'unió comporta la funció coordinada de més de 200 proteïnes en la síntesi i processament de quatre molècules d'ARN ribosòmic, així com la unió d'aquestes molècules d'ARN ribosòmic amb proteïnes ribosomals.
Localització dels ribosomes
modificaEls ribosomes es classifiquen en ribosomes lliures o ribosomes de membrana. Només difereixen en la seva distribució espacial; són idèntics d'estructura. Si es troben o no adherits a la membrana depèn de la presència d'una seqüència senyal de direcció al reticle endoplasmàtic (RE) que pot portar la proteïna que està essent sintetitzada, pel que un mateix ribosoma pot trobar-se en la membrana del reticle quan està formant una proteïna o lliure en el citosol quan n'està formant una altra.
Ribosomes lliures
modificaEls ribosomes lliures poden moure's per tot el citosol, però no pel nucli cel·lular o altres orgànuls. Les proteïnes formades per ribosomes lliures són alliberades al citosol i utilitzades dins les cèl·lules. Com que el citosol conté altes concentracions de glutatió i és, conseqüentment, un ambient reductor, les proteïnes que tenen enllaços disulfur, formades per l'oxidació de residus de cisteïna, no poden ser sintetitzades en aquest compartiment.
Ribosomes de membrana
modificaQuan els ribosomes comencen a sintetitzar proteïnes necessàries en orgànuls concrets, el ribosoma que s'encarrega de la proteïna en qüestió pot adherir-se a una membrana. En cèl·lules eucariotes això passa en una regió del reticle endoplasmàtic anomenat reticle endoplasmàtic rugós. Les noves cadenes polipeptídiques són inserides directament dins el reticle endoplasmàtic pel ribosoma i són transportades des d'allà cap a altres destinacions a través de la via secretora. Els ribosomes de membrana sovint sintetitzen proteïnes que seran dirigides a la membrana plasmàtica o expulsades de la cèl·lula per exocitosi.
Estructura
modificaLes subunitats de ribosomes procariotes i eucariotes són força similars.[8] La unitat de mesura és l'Svedberg, mesura del grau de sedimentació en una centrifugació més que de la mida, raó per la qual els noms dels fragments no són la suma d'aquests (la subunitat 70s està composta per 50s i 30s).
Els organismes procariotes tenen ribosomes de 70s, cadascun consistent en una subunitat petita de 30s i una de gran de 50s. Aquesta subunitat gran està formada per una subunitat d'ARN de 5s (consistent en 120 nucleòtids), una de 23s (de 2900 nucleòtids) i 31 proteïnes. La subunitat de 30s té una subunitat de 1540 nucleòtids d'ARN de 16s enllaçat a 21 proteïnes.[9] El nivell d'afinitat pels llocs d'unió de l'ARNt amb els ribosomes d'E. Coli van permetre la identificació de les proteïnes A i P normalment associades amb l'activitat de la peptidil transferasa; les proteïnes etiquetades són les L27, L14, L15, L16, L2; La L27 es troba localitzada a la part donadora tal com fou mostrat per E. Collatz and A.P. Czernilofsky et al. (FEBS articles, 63 pp 283-286, 1976, Proc. Natl. Sci., USA, 71, pp230-234, 1974). Les proteïnes involucrades en la iniciació de la traducció, les S1 i S21, estan associades amb l'extrem 3' de l'ARN ribosomal de 16s, com determinà A.P. Czernilofsky et al. per l'encreuament de proteïnes d'ARN amb la seqüència Shine-Dalgarno (FEBS articles, 58, pp281-284, 1975).
Els organismes eucariotes tenen ribosomes de 80s, cadascun consistent en una subunitat petita de 40s i una de gran de 60s. La seva subunitat gran està composta per ARN de 5s (120 nucleòtids), ARN de 28s (4700 nucleòtids), ARN de 5.8s (160 nucleòtids) i unes 49 proteïnes. La subunitat de 40s té un ARN de 18s (1900 nucleòtids) i unes 33 proteïnes.[9] La identificació dels llocs d'enllaç de l'ARN de transferència en ribosomes de fetges de rata va ser duta a terme per A.P. Czernilofsky et al. 1977, amb moltes proteïnes incloent L32/33, L36, L21, L23, L28/29 i L13 (Molec. Gen. Genet. 153, pp231-235, 1977).
Els ribosomes trobats en cloroplasts i mitocondris d'eucariotes consisteixen en una subunitat petita i una de gran unides per proteïnes en una partícula de 70s.[9] Es creu que aquests orgànuls són descendents de bacteris (vegeu la teoria endosimbiòtica) i com a tals els seus ribosomes són similars als dels bacteris.[10]
Els ribosomes varis comparteixen una estructura central força similar tot i les grans diferències de mida. La majoria de l'ARN està altament organitzat en diverses estructures terciàries conegudes com a “tertiary structural motifs”. L'ARN extra dels ribosomes més grans és en llargues insercions que surten de l'estructura principal sense trencar-la o canviar-la.[9] Tota l'activitat catalítica del ribosoma és duta a terme per l'ARN; les proteïnes resideixen a la superfície i sembla que estableixin l'estructura.[9]
Les diferències entre ribosomes bacterians i eucariotes són explotades per químics farmacèutics per crear antibiòtics que puguin destruir infeccions bacterianes sense malmetre les cèl·lules de la persona infectada. Degut a les diferències de les seves estructures, els ribosomes de 70s dels bacteris són vulnerables a aquests antibiòtics mentre que els ribosomes de 80s dels eucariotes no ho són.[11] Tot i que els mitocondris posseeixen ribosomes similars als dels bacteris, aquests no són afectats per aquests antibiòtics perquè estan envoltats d'una doble membrana que no admet aquests medicaments fàcilment dins l'orgànul.[12]
Estructura d'alta resolució
modificaL'estructura molecular general del ribosoma ha estat coneguda des de principis dels anys 70. A principis de 2000 l'estructura va ser aconseguida a altes resolucions, en l'ordre de pocs Armstrongs.
Els primers documents que donaven l'estructura del ribosoma a resolució atòmica van ser publicats en una ràpida successió a finals del 2000. Primer va ser publicada la unitat de 50s (procariotes grans) dels arqueans Haloarcula marismortui.[13] Poc després ho va ser l'estructura de la subunitat de 30s de Thermus thermophilus[14] i al cap de poc, va ser publicada una estructura molt més detallada.[15] Aquests estudis estructurals van ser premiats amb el Premi Nobel de química de 2009. A principis de l'any següent (maig de 2001) aquests estudis coordinats van servir per reconstruir l'estructura sencera de la subunitat de 70s de T. thermophilus amb una resolució de 5.5 Armstrongs.[16]
Dos documents van ser publicats el novembre de 2005 amb estructures de ribosomes de 70s d'Escherichia coli. Les estructures vacants de ribosomes van ser determinades amb una resolució de 3.5 Armstrongs utilitzant cristal·lografia de rajos x.[17] Dues setmanes més tard, una estructura detallada per microscòpia electrònica de criofractura va representar el ribosoma amb una resolució entre 11 i 15 Armstrongs en l'acte de passar una nova proteïna sintetitzada per un canal translocador de proteïnes.[18]
Primer les estructures atòmiques del complex ribosòmic de molècules d'ARNt i ARNm van poder ser observades utilitzant cristal·lografia de rajos x pels dos grups independentment, amb una resolució de 2.8[19] i 3.7[20] Armstrongs. Aquestes estructures permeten veure els detalls de les interaccions dels ribosomes de Thermus thermophilus amb enllaços d'ARNm i amb enllaços ARNt a parts del ribosoma. Les interaccions del ribosoma amb ARNm llargs que contenen seqüències Shine-Dalgamo van ser visualitzats poc després amb una resolució de 4.5 a 5.5 Armstrongs.[21]
Funció
modificaEls ribosomes són les bèsties de càrrega de la biosíntesi de les proteïnes, el procés de transcripció de l'ARNm en proteïna. L'ARNm consta d'una sèrie de codons que dicten al ribosoma la seqüència de l'aminoàcid que es necessita per fabricar la proteïna. Utilitzant l'ARNm com a patró, el ribosoma creua cada codó (3 nucleòtids) d'ARNm, emparellant-lo amb l'aminoàcid adequat de l'ARNt. Les molècules d'ARN de transferència contenen un anticodó complementari a l'extrem final i l'aminoàcid adequat a l'altre extrem. La subunitat petita del ribosoma s'uneix al codó AUG en l'ARNm i recluta la subunitat ribosòmica gran. El ribosoma llavors conté tres llocs d'unió d'ARN, designats A, P i E. L'A uneix un aminoacil-RNAt (un ARNt unit a un aminoàcid); el P uneix un peptidil-RNAt (un ARNt unit a un pèptid que s'està sintetitzant), i l'E que uneix un ARNt lliure abans que abandoni el ribosoma. La síntesi de proteïnes comença al codó d'inici AUG, proper a l'extrem 5' final de l'ARNm. L'ARNm s'uneix al lloc P del primer ribosoma. El ribosoma està disponible per identificar el codó inicial a través de l'ús de la seqüència Shine-Dalgarno de l'ARNm a les procariotes i Kozak box a les eucariotes.
La proteïna és una cadena formada per aminoàcids. Entre els éssers vius s'han descobert fins ara 22 aminoàcids transcripcionals, encara que els més usuals -els únics en els humans- són només 20. El procés és el següent:
- El ribosoma llegeix tres lletres del codi genètic que ha transportat en ARN. (Tres lletres codifiquen un aminoàcid i es diuen codó).
- Escull l'aminoàcid corresponent a aquestes tres lletres.
- Llegeix les següents tres lletres (el següent codó) i ensambla l'aminoàcid corresponent al costat de l'anterior...
- I així fins que arriba al codó que dona ordre d'acabar la síntesi.
Per exemple:
L'ARN és aquest:
AUGGCCAACGGCAUGCCUACUUAA
- AUG li indica que ha de començar a ensamblar la proteïna; és un codó d'inici (la interpretació d'aquest pot ser força diferent dependent de l'organisme, n'hi ha que ensamblen una metionina que després s'elimina).
- GCC és Alanina. Agafa Alanina (un aminoàcid) i el subjecta.
- AAC és Arginina, la posa al costat de l'Alanina.
- GGC és Glicina, l'ensambla al costat de l'Arginina.
- AUG era el símbol d'inici, però ja ha començat; així que ho interpreta com a Metionina. Posa l'aminoàcid Metionina ensamblat amb la Glicina.
- CCU és Prolina. Ensambla la Prolina a la Metionina.
- ACU és Serina. Ensambla la serina amb la Prolina.
- UAA és un Codó STOP. Deixa d'ensamblar la proteïna.
Per tant la proteïna ensamblada ha estat: (Metionina)-Alanina-Arginina-Glicina-Metionina-Prolina-Serina
Origen
modificaS'especula que el ribosoma podria haver aparegut per primera vegada en el context del món d'ARN, com a complex autoreplicatiu que després va desenvolupar l'habilitat de sintetitzar proteïnes a mesura que els aminoàcids van començar a aparèixer.[22] Alguns estudis suggereixen que els antics ribosomes només estaven formats per ARNr, que podia haver adquirit la capacitat de formar enllaços peptídics.[23][24] Per altra banda, en aquests antics ribosomes com a complexos autoreplicatius, l'ARNr, apart d'una funció estructural, també la tindria a nivell informacional i catalític, atès que podria codificar tant els ARNt com les proteïnes necessàries per a la replicació del ribosoma.[25] Aquells organismes cel·lulars hipotètics que tindrien un ARN autoreplicatiu, però sense cap ADN, són conegut com a ribocits (o ribocel·lules).[26][27]
A mesura que els aminoàcids començaven a abundar en aquest món d'ARN sota condicions prebiòtiques,[28][29] llurs interaccions amb els ARN catalítics van augment l'abast i l'eficiència de la funció de les molècules d'ARN. Per tant, allò que va portar els antics ribosomes de ser un complex autoreplicatiu a la seva forma actual de centre traduccional pot haver estat la pressió selectiva per incorporar proteïnes en els mecanismes d'autoreplicació per tal d'augmentar-ne la capacitat.
Premi Nobel
modificaJuntament amb Albert Claude i Christian de Duve, George Emil Palade va ser premiat amb el Premi Nobel en Fisiologia i Medicina, el 1974, pel descobriment dels ribosomes.[30] El Premi Nobel en Química 2009 va ser atorgat als Drs. Venkatraman Ramakrishnan, Thomas A. Steitz i Ada E. Yonath per "l'estudi de l'estructura i funció del ribosoma".[31]
Notes i referències
modifica- ↑ ^ Korostelev AA (August 2011). "Structural aspects of translation termination on the ribosome". RNA (New York, N.Y.) 17 (8): 1409–21. doi:10.1261/rna.2733411. PMID: 21700725. http://rnajournal.cshlp.org/cgi/pmidlookup?view=long&pmid=21700725.
- ↑ ^ Benne R, Sloof P (1987). "Evolution of the mitochondrial protein synthetic machinery". BioSystems 21 (1): 51–68. doi:10.1016/0303-2647(87)90006-2. PMID: 2446672
- ↑ ^ "Ribosomes". http://www.cs.stedwards.edu/chem/Chemistry/CHEM43/CHEM43/Ribosomes/Ribosome.HTML Arxivat 2009-03-20 a Wayback Machine.. Retrieved 2011-04-28.
- ↑ ^ Rodnina MV, Beringer M, Wintermeyer W (2007). "How ribosomes make peptide bonds". Trends Biochem. Sci. 32 (1): 20–6. doi:10.1016/j.tibs.2006.11.007. PMID: 17157507
- ↑ ^ Cech T (2000). "Structural biology. The ribosome is a ribozyme". Science 289 (5481): 878–9. doi:10.1126/science.289.5481.878. PMID: 10960319
- ↑ ^ PALADE GE (January 1955). "A small particulate component of the cytoplasm". J Biophys Biochem Cytol 1 (1): 59–68. PMC 2223592. PMID: 14381428. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=2223592.
- ↑ ^ Roberts, R. B., editor. (1958) "Introduction" in Microsomal Particles and Protein Synthesis. New York: Pergamon Press, Inc.
- ↑ # ^ a b Schluenzen F, Tocilj A, Zarivach R, Harms J, Gluehmann M, Janell D, Bashan A, Bartels H, Agmon I, Franceschi F, Yonath A (2000). "Structure of functionally activated small ribosomal subunit at 3.3 angstroms resolution". Cell 102 (5): 615-23. doi:10.1016/S0092-8674(00)00084-2. PMID: 11007480
- ↑ 9,0 9,1 9,2 9,3 9,4 ^ a b c d e f The Molecular Biology of the Cell, fourth eddition. Bruce Alberts, et al. Garland Science (2002) pg. 342 ISBN 0-8153-3218-1
- ↑ # ^ The Molecular Biology of the Cell, fourth edition. Bruce Alberts, et al. Garland Science (2002) pg. 808 ISBN 0-8153-3218-1
- ↑ ^ Recht MI, Douthwaite S, Puglisi JD (1999). "Basis for bacterial specificity of action of aminoglycoside antibiotics". EMBO J 18 (11): 3133–8. doi:10.1093/emboj/18.11.3133. PMC 1171394. PMID: 10357824. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=1171394.
- ↑ ^ O'Brien, T.W., The General Occurrence of 55S Ribosomes in Mammalian Liver Mitochondria. J. Biol. Chem., 245:3409 (1971).
- ↑ ^ a b Ban N, Nissen P, Hansen J, Moore P, Steitz T (2000). "The complete atomic structure of the large ribosomal subunit at 2.4 ångström resolution". Science 289 (5481): 905–20. doi:10.1126/science.289.5481.905. PMID: 10937989
- ↑ ^ a b Schluenzen F, Tocilj A, Zarivach R, Harms J, Gluehmann M, Janell D, Bashan A, Bartels H, Agmon I, Franceschi F, Yonath A (2000). "Structure of functionally activated small ribosomal subunit at 3.3 angstroms resolution". Cell 102 (5): 615-23. doi:10.1016/S0092-8674(00)00084-2. PMID: 11007480
- ↑ ^ Wimberly BT, Brodersen DE, Clemons WM, et al. (September 2000). "Structure of the 30S ribosomal subunit". Nature 407 (6802): 327-39. doi:10.1038/35030006. PMID: 11014182
- ↑ ^ Yusupov MM, Yusupova GZ, Baucom A, et al. (May 2001). "Crystal structure of the ribosome at 5.5 A resolution". Science 292 (5518): 883–96. doi:10.1126/science.1060089. PMID: 11283358
- ↑ ^ Schuwirth BS, Borovinskaya MA, Hau CW, et al. (November 2005). "Structures of the bacterial ribosome at 3.5 A resolution". Science 310 (5749): 827–34. doi:10.1126/science.1117230. PMID: 16272117
- ↑ ^ Mitra K, Schaffitzel C, Shaikh T, et al. (November 2005). "Structure of the E. coli protein-conducting channel bound to a translating ribosome". Nature 438 (7066): 318–24. doi:10.1038/nature04133. PMC 1351281. PMID: 16292303. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=1351281.
- ↑ ^ Selmer M, Dunham CM, Murphy FV, et al. (September 2006). "Structure of the 70S ribosome complexed with mRNA and tRNA". Science 313 (5795): 1935–42. doi:10.1126/science.1131127. PMID: 16959973
- ↑ ^ Korostelev A, Trakhanov S, Laurberg M, Noller HF (September 2006). "Crystal structure of a 70S ribosome-tRNA complex reveals functional interactions and rearrangements". Cell 126 (6): 1065–77. doi:10.1016/j.cell.2006.08.032. PMID: 16962654
- ↑ ^ Yusupova G, Jenner L, Rees B, Moras D, Yusupov M (November 2006). "Structural basis for messenger RNA movement on the ribosome". Nature 444 (7117): 391–4. doi:10.1038/nature05281. PMID: 17051149
- ↑ Noller, Harry F. «Evolution of Protein Synthesis from an RNA World» (en anglès). Cold Spring Harbor Perspectives in Biology, 4, 4, 01-04-2012, pàg. a003681. DOI: 10.1101/cshperspect.a003681. ISSN: 1943-0264. PMID: 20610545.
- ↑ Zimniak, L.; Hoffarth, V.; Noller, H. F. «Unusual resistance of peptidyl transferase to protein extraction procedures» (en anglès). Science, 256, 5062, 05-06-1992, pàg. 1416–1419. DOI: 10.1126/science.1604315. ISSN: 0036-8075. PMID: 1604315.
- ↑ Lowry, C. V.; Traub, P.; Ozaki, M.; Mizushima, S.; Nomura, M. «Structure and Function of Ribosomes and Their Molecular Components» (en anglès). Cold Spring Harbor Symposia on Quantitative Biology, 34, 01-01-1969, pàg. 49–61. DOI: 10.1101/SQB.1969.034.01.009. ISSN: 0091-7451. PMID: 4909519.
- ↑ Root-Bernstein, Meredith; Root-Bernstein, Robert «The ribosome as a missing link in the evolution of life». Journal of Theoretical Biology, 367, 21-02-2015, pàg. 130–158. DOI: 10.1016/j.jtbi.2014.11.025. ISSN: 0022-5193.
- ↑ Yarus, Michael «Primordial Genetics: Phenotype of the Ribocyte». Annual Review of Genetics, 36, 1, 01-12-2002, pàg. 125–151. DOI: 10.1146/annurev.genet.36.031902.105056. ISSN: 0066-4197.
- ↑ Forterre, Patrick; Krupovic, Mart. «The Origin of Virions and Virocells: The Escape Hypothesis Revisited». A: Viruses: Essential Agents of Life, 2012, p. 43–60. DOI 10.1007/978-94-007-4899-6_3. ISBN 978-94-007-4898-9.
- ↑ «The coevolutionary roots of biochemistry and cellular organization challenge the RNA world paradigm». Journal of Molecular Microbiology and Biotechnology, 23, 1–2, 2013, pàg. 152–77. DOI: 10.1159/000346551. PMID: 23615203.
- ↑ «Genetics first or metabolism first? The formamide clue». Chemical Society Reviews, 41, 16, agost 2012, pàg. 5526–65. DOI: 10.1039/c2cs35066a. PMID: 22684046.
- ↑ # ^ Palade.
- ↑ ^ 2009 Nobel Prize in Chemistry, Nobel Foundation.
Vegeu també
modifica