Virus de la febre hemorràgica de Crimea-Congo
El virus de la febre hemorràgica de Crimea-Congo (VFHCC) és un virus de la família Bunyaviridae i del gènere Nairovirus que representa una amenaça important pels humans. Es transmet principalment a través de picades de paparres dures (Ixodidae) dels gèneres Hyalomma (considerat el vector més eficaç del VFHCC), Haemaphysalis, Rhipicephalus[1] i Dermacentor,[2] tot i que també es pot donar el contagi per contacte directe amb els hostes d'aquests àcars, que són grans herbívors domèstics, com vaques, cabres i ovelles, i animals salvatges com llebres, guineus o eriçons.[3] En humans, és un virus que provoca brots greus de febre hemorràgica vírica i de fet, la taxa de mortalitat d'aquests brots pot arribar fins al 40% (10%-40%).[4] És un virus relativament jove. Els estudis filogenètics més recents han rastrejat la seva empremta genòmica fins a Àfrica, uns 1000-5000 anys BP.[5] S'han identificat pèptids del VFHCC a restes humanes celtes d'un poblat de Heuneburg (Alemanya), datat uns 750–400 anys a. de la n. e. (Edat del Ferro primerenca).[6] La Febre hemorràgica de Crimea-Congo (FHCC) és una malaltia viral zoonòtica molt estesa mundialment, endèmica d'Àfrica, Àsia, Europa de l'est i l'Orient Mitjà.[7] No presenta símptomes en els animals infectats però representa una greu amenaça pels éssers humans, sobretot pels productors i altres treballadors agrícoles, veterinaris, treballadors de laboratori i personal hospitalari.[8]
| Orthonairovirus haemorrhagiae | |
|---|---|
 | |
| Dades | |
| Malaltia | febre hemorràgica de Crimea-Congo |
| Taxonomia | |
| Família | Bunyaviridae |
| Gènere | Nairovirus |
| Espècie | Orthonairovirus haemorrhagiae |
| Nomenclatura | |
| Sinònims | |
 | |
| Tipus | infecció vírica, malaltia rara de la pell, infecció cutània, infecció per Bunyaviridae, febre hemorràgica vírica, malaltia i malalties propenses a pandèmies i epidèmies |
|---|---|
| Epònim | Crimea i Congo |
| Especialitat | infectologia |
| Clínica-tractament | |
| Símptomes | febre, calfred, cefalàlgia, miàlgia, artràlgia, flatulència, nàusea, vòmit, dolor abdominal, hiperèmia, conjuntivitis, xerostomia, bradicàrdia, hipotensió arterial, petèquia, hematoma, hemorràgia, hematúria, oligúria, Anúria, taquicàrdia, signes de meningisme, cianosi, icterícia i raquiàlgia |
| Exàmens | exploració física, hemograma, anàlisi d'orina, anàlisi de sang, punció lumbar i reacció en cadena de la polimerasa |
Medicació | |
| Patogènesi | |
| Transmissió patògena | transmissió per paparres, Hyalomma i transmissió per contacte |
| Causat per | virus de la febre hemorràgica de Crimea-Congo |
| Classificació | |
| CIM-11 | 1D49 |
| CIM-10 | A98.098.0 |
| CIM-9 | 065.0065.0 |
| Recursos externs | |
| DiseasesDB | 31969 |
| MeSH | D006479 |
| Orphanet | 99827 |
| UMLS CUI | C0019099 |
| DOID | DOID:12287 |
Història
modificaEl primer cop que es va descriure el VFHCC va ser el segle xii a Tajikistan, quan es va detectar una febre hemorràgica que es caracteritzava per la presència de sang a l'orina, al recte, a les genives, i a la cavitat abdominal i vòmits i es va dir que era causada per la picada d'una paparra que parasitava les aus.[9]
Però la primera vegada que es va detectar el virus de la febre hemorràgica de Crimea-Congo pensant que era un virus sense descobrir encara va ser el 1944 a 200 soldats soviètics que estaven a la península de Crimea.[10] Es va aconseguir conèixer l'etiologia gràcies a la inoculació del virus a "voluntaris", però no es va aconseguir aïllar fins al 1967 (ho va fer el científic soviètic Chumakov).
Uns mesos abans, s'havien fet publicacions sobre un virus anomenat Congo-Virus, que havia estat aïllat a partir de persones infectades a aquella zona. Chumakov va enviar el seu virus aïllat als laboratoris on s'estava treballant amb el virus i es varen fer proves. També es va trobar una mostra a Uganda, que va ser comparada amb la del Congo al Rockefeller Foundation Virus Laboratory, i es va veure que les dues mostres eren iguals. Més tard, Chumakov va enviar el virus trobat a Crimea i també es va veure que eren indistingibles antigènicament[11][12]
Quan es van adonar que eren el mateix virus, es varen unificar els noms i va passar a anomenar-se CHF-Congo Virus, però molts autors han adoptat el nom de virus de la febre hemorràgica de Crimea-Congo.[9]
Un cas mortal per aquesta malaltia vírica es donà l'estiu del 2008 a una zona muntanyosa de Ròdope (Grècia oriental).[13]
Al nostre entorn proper, el VFHCC va ser identificat a paparres de cérvol comú l'any 2010, a la província de Càceres.[14] Els resultats dels estudis genòmics van coincidir amb els de les paparres d'ocells migradors d'Àfrica del Nord.[15] La primera mort enregistrada a l'Estat Espanyol i a Europa Occidental,[16] causada per la infecció del VFHCC va ser al setembre de 2016,[17] transmessa per la picada d'una paparra a la província d'Àvila. Una infermera que assistí el cas va contagiar-se amb el virus i fou ingressada en una unitat especial d'aïllament. Aquest primer cas autòcton va comportar un seguiment epidemiològic per part del Ministeri de Sanitat[18] i canvis en els protocols sanitaris de tota la UE.[19] Els estudis moleculars (paparres) i serològics (humans) més recents, indiquen que el risc d'adquisició de la infecció per VFHCC a la península Ibèrica és baix.[20] Un treball multicèntric de seguiment publicat pel MSSSI l'abril del 2017, va indicar la presència del VFHCC en paparres d'animals salvatges a set comarques d'Extremadura, Castella-la Manxa, Castella i Lleó i Madrid. De més de 9.500 paparres analitzades, es detectà el virus a 128 exemplars.[21] L'estudi epidemiològic i clínic del curs de la infecció en aquests casos autòctons ha demostrat que el virus dels dos malalts era idèntic i compartia l'empremta genètica d'una línia africana sense relació amb la crimeana present a Europa Oriental, fet que indica un canvi en la distribució geogràfica del VFHCC.[22]
Segons les darreres informacions de l'OMS, el nombre de països amb casos registrats i la morbiditat de les infeccions pel VFHCC ha augmentat significativament a les regions del Mediterrani Oriental, a causa d'un increment del transport de bestiar (un fet que afavoreix el contagi de les aus migratòries) i les modificacions ambientals.[23] A Turquia, lloc de pas de moltes aus migratòries, s'ha detectat el VFHCC a balquers i pit-roigs europeus. Al delta del riu Kızılırmak, una zona d'importància ecològica, es creu que la convivència d'espècies residents i espècies migratòries afavoreix l'extensió del virus.[24]
El gener de 2017, els experts de l'organisme de l'OMS encarregat de coordinar els treballs sanitaris d'I+D a nivell mundial van incloure la febre hemorràgica per VCC en la llista de malalties prioritàries.[25]
Caracterització
modificaEs tracta d'un virus ARN monocatenari negatiu de la família Bunyaviridae i del gènere Nairovirus.[26]
| Classificació taxonómica | |
|---|---|
| Grup | Grup V ((-)ssRNA) |
| Família | Bunyaviridae |
| Gènere | Nairovirus |
| Espècie | Virus de la febre hemorràgica de Crimea Congo |
Morfologia
modificaEls virions són esfèrics, d'aproximadament 100 nm de diàmetre i estan recoberts per una bicapa lípidica de 5-7 nm de gruix, de la qual sobresurten unes glucoproteïnes de 8-10 nm. El VFHCC té tres tipus proteïnes estructurals: dos tipus de glucoproteïnes que s'insereixen a la càpside (Gn i Gc) i les proteïnes que formen la nucleocàpside, a més d'un llarg pèptid que és l'ARN-polimerasa ARN depenent.
Genoma
modificaÉs un virus amb ARN circular de cadena simple segmentat de polaritat negativa en tres segments de cadena negativa :S(small), M(middle) i L(large), que codifiquen la nucleocàpside, les glucoproteïnes envolvents de la càpside (primer són fabricades com un precursor, que després és tallat i dona lloc a Gn i Gc) i l'ARN polimerasa ARN depenent, respectivament. Aquests segments d'ARN formen complexos amb les glicoproteïnes de la nucleocàpside formant ribonucleocàpsides (necessàries perquè el virus sigui infectiu (virió).[27] En ser un virus amb genoma segmentat es poden generar noves variants genètiques per combinació dels segments de dos soques diferents que hagin coinfectat a un mateix individu (infecció doble). Això té implicacions patogèniques i epidemiològiques i contribueix a la gran variabilitat genòmica del VFHCC.[28]
Cicle de replicació
modificaEl VFHCC té el cicle típic de la família Bunyaviridae. Primer de tot els virions ataquen els receptors de la superfície cel·lular (receptors clatrina dependents) i es produeix una endocitosi mediada per receptor. Es produeix una baixada de pH que fa que les glucoproteïnes de la càpside canviïn de conformació, cosa que provoca que els endosomes es fusionin amb l'embolcall del virus permetent l'entrada de la ribonucleocàpside i de l'ARN polimerasa ARN depenent al citoplasma cel·lular. Quan ja s'ha dissociat la nucleocàpside, comença la replicació i l'ARN polimerasa ARN depenent genera ARNm (per la transcripció de les proteïnes virals) i ARN complementari (ARNc), intermediari de l'ARN víric. La formació de les glucoproteïnes té lloc al reticle endoplasmàtic on el precursor és tallat i es formen Gn i Gc. Aquestes glucoproteïnes són transportades a l'aparell de Golgi, on es produirà l'acoblament de l'ARN amb la càpside amb Gn i Gc inserides i, finalment, s'exocitarà la partícula vírica infectiva.[29] També és possible que el virió s'acobli a la membrana plasmàtica i es produeixi l'exocitosi directament d'allà[30]
Genètica
modificaEl VFHCC va aparèixer fa uns 3100-3500 anys.[31] És un dels arbovirus amb més diversitat genètica. Si ens basam en la seqüenciació de l'ARN, trobam set soques: Àfrica 1 (Senegal), Àfrica 2 (República Democràtica del Congo i Sud-àfrica), Àfrica 3 (sud i oest d'Àfrica), Europa 1 (Albània, Bulgària, Kosovo, Rússia i Turquia), Europa 2 (Grècia), Àsia 1 (centre-est, Iran i Pakistan) i Àsia 2 (Xina, Kazakhstan, Tajikistan i l'Uzbekistan).[32] Aquesta gran diversitat gènica, no present a altres virus de la seva família, es fonamenta en la extraordinària capacitat de mutació del VFHCC mentre infesta els hostes invertebrats (paparres).[33] A Kosovo, per exemple, la coexistència de virus de les soques Europa 1 i 2 ha donat lloc a diferents subsoques: Kosovo I, Kosovo II, Kosovo IIa i Kosovo IIb.[34] El VFHCC és el virus causal de febre hemorràgica transmès per paparres amb major presència internacional. Més de 30 països tenen zones endèmiques i pocs d'ells laboratoris amb un nivell de bioseguretat 4 que faci possible la recerca de vacunes o antivirals contra la malaltia.[35]
Podem identificar en una mateixa zona geogràfica dos genotips diferents de VFHCC. Això és conseqüència de la capacitat de les aus migratòries de transportar el vector (diverses espècies de paparres del gènere Hyalomma) a altres latituds i així trobar diferents genotips a territoris petits.[36] Algunes soques del virus tenen un endemisme molt marcat i semblen no tenir la propietat de ser transportades per les paparres de les aus.[37]
El segment d'ARN L no s'ha seqüenciat tant com els segments S i M, però hi ha evidències que S i L han tengut la mateixa evolució històrica. És diferent el cas del segment M. Això s'explica pel fet que el VFHCC és capaç de recombinar-se amb altres virus quan coinfecten la mateixa cèl·lula i s'ha observat que la freqüència de recombinacions és superior en el segment M que en S i L.[32] Aquestes característiques especials podrien ser molt importants pel desenvolupament d'una vacuna eficaç.[38]
Simptomatologia / Quadre clínic
modificaDesprés de la picada de paparra, la fase d'incubació és normalment d'1-3 dies, amb un màxim de 9 dies. El període d'incubació després del contacte amb sang o teixits infectats és normalment de 5 o 6 dies, amb un màxim documentat de 13 dies.[39]
El primer senyal de febre hemorràgica de Crimea Congo és una aparició sobtada de febre i d'altres símptomes inespecífics com calfreds, un mal de cap intens, marejos, fotofòbia, dolor a la nuca, miàlgia i mal a les articulacions. La febre pot ser molt alta. També són comuns els símptomes gastrointestinals, com nàusees, vòmits, diarrea no sanguinolenta, dolor abdominal i mal de coll al principi, seguit de canvis bruscs d'humor i confusió.[40] Al cap de dos a quatre dies, l'agitació pot donar pas a la somnolència, la depressió i la debilitat, i pot aparèixer dolor abdominal en el quadrant superior dret, amb hepatomegàlia perceptible.
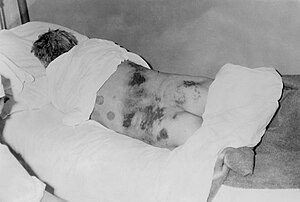
Altres possibles signes clínics inclouen taquicàrdies, adenopaties (inflamació dels ganglis limfàtics), i erupcions petequials (hemorràgies cutànies de petit diàmetre) en mucoses internes, com la boca i la gola, i també la pell. Les petèquies poden donar lloc a hemorràgies subcutànies més grans anomenades hematomes, així com altres fenòmens hemorràgics.[39]
Als 4-5 dies es produeixen hemorràgies variades: epistaxis, hematèmesis, hematúries, hemorràgies gingivals, vaginals o per altres orificis naturals. Poden haver hemorràgies internes (dins d'una cavitat o espai corporal), incloent-hi intracranials i intraperitoneals. Els pacients molt greus poden desenvolupar un problema hepatorenal i pulmonar cap al 5é dia i provocar gradualment somnolència, estupor i coma.
Normalment hi ha signes d'hepatitis, i els pacients molt greus poden patir un ràpid deteriorament renal, o insuficiència hepàtica, o pulmonar sobtada després del cinquè dia de malaltia. Les alteracions pulmonars més freqüents són: infiltrat inflamatori parenquimatós, hemorràgies alveolars, vessament pleural i atelèctasi (col·lapse del pulmó).[41]
S'ha demostrat una elevada concentració de l'hormona irisina (secretada pels músculs després de la proteòlisi de la fibronectina tipus III i que té un paper important en la regulació de la termogènesi), a la sang dels malalts infectats. Això pot explicar en bona part els danys endotelials generalitzats i les grans hemorràgies que la malaltia provoca.[42]
En pacients que sobreviuen, la recuperació comença de 10 a 20 dies després de l'aparició de la malaltia. La recuperació és normalment completa però lenta i pot durar fins a un any.[40]
La taxa de mortalitat de la Febre hemorràgica de Crimea Congo és aproximadament d'un 30%, i la mort sobrevé durant la segona setmana.[39]
La infecció pel VFHCC en dones embarassades no és freqüent. Comporta una mortalitat materna superior a la mitjana (34%) i fetal/perinatal (58%) molt alta. La majoria dels casos deriven de transmissió per paparres, si bé un percentatge considerable es deu a transmissions no vectorials. Ja que aquests tipus de processos impliquen procediments assistencials i quirúrgics importants, el risc d'ocasionar infeccions nosocomials secundàries entre el personal mèdic i/o altres pacients és elevat.[43]
Diagnòstic
modificaLa realització d'un diagnòstic precoç de la malaltia és imprescindible per a garantir la supervivència dels afectats i preveure una infecció nosocomial.
Mostra òptima per a l'aïllament del Virus de la Febre Hemorràgica de Crimea-Congo
modificaLes mostres que es poden remetre poden provenir d'un animal viu o mort. En el cas d'un animal viu s'empra sang coagulada per a la realització de serologia, sang anticoagulada per altres proves complementàries com poden ser un hemograma també plasma i teixits obtinguts per biòpsia; contràriament, si la mostra prové d'un animal mort la mostra serà obtinguda per biòpsia de teixits com el pulmó, fetge, melsa, medul·la òssia, ronyó o cervell.[44]
L'aïllament del virus
modificaL'aïllament del virus de la Febre Hemorràgica de Crimea-Congo ha de realitzar-se en un laboratori de bioseguretat de nivell 4 tot i que en cas que el virus hagi sigut inactivat prèviament amb viricides o raigs gamma poden manipular-se en un entorn de bioseguretat bàsic.[45] Aquest aïllament es fa mitjançant cultius cel·lulars i és el mètode més ràpid i senzill pel diagnòstic d'aquesta malaltia tot i que sols és eficaç quan hi ha una elevada concentració de virus i durant els primers cinc dies de la malaltia. Si optem per diagnosticar la malaltia amb aquest mètode els resultats s'aconsegueixen en un període de 2 a 5 dies però com que l'efecte citopàtic d'aquest virus es veu reduït després de l'aïllament s'opta per identificar-lo mitjançant immunofluorescència o anticòs monoclonal. Una altra opció, però més orientada a la investigació i la recerca és la inoculació animal a ratolins perinatals; aquest mètode és molt més sensible que un cultiu cel·lular i, a més a més permet detectar el virus durant un període perllongat.
Identificació del virus mitjançant procediments d'anàlisi immunològica
modificaEls procediments d'anàlisi immunològica es basen en la unió entre els antígens i els anticossos que es produeixen en l'organisme davant d'una infecció, i en el fet de poder repetir aquestes situacions al laboratori, és a dir, es provoquen reaccions antigen-anticòs per posar en evidència la presència de l'antigen o de l'anticòs, segons el cas.
Per a la identificació d'aquest virus es poden triar diferents proves d'anàlisi immunològica com són la prova d'immunoadsorció enzimàtica (ELISA) i la immunofluorescència. Les immunoglobulines G i M es detecten mitjançant immunoadsorció enzimàtica i la immunofluorescència té l'avantatge que es pot emprar set dies després de l'inici de la malaltia. Normalment, s'usa la ELISA com a anàlisi immunològica degut a la seva elevada sensibilitat i especificitat.
Aïllaments moleculars
modificaLes proves de diagnòstic molecular són una gran eina pel diagnòstic del VFHCC degut a la rapidesa, elevada sensibilitat i especificitat per a diagnosticar la presència del virus. La prova més usada en l'aïllament molecular és l'anomenada Reacció en Cadena de la Polimerasa amb transcriptasa inversa.
Tractament
modificaEl tractament dels infectats pel virus de la Febre Hemorràgica de Crimea-Congo és de sosteniment i inclou transfusions de trombòcits, plasma congelat i concentrat d'hematies. Durant el tractament s'han de realitzar periòdicament analítiques bàsiques d'hematologia com són l'hemograma i bioquímica general. També s'ha de vigilar possibles zones d'hemorràgia i administrar inhibidors de la bomba de protons com per exemple l'Omeprazole i antihistamínics de segona generació, com per exemple la Cetirizina. En alguns casos s'ha d'administrar Ribavirina i/o T-705 (uns nucleòsids sintètics antivirals),[46] l'únic tractament disponible. Però, no existeixen assajos clínics que demostrin la seva eficàcia perquè sols s'ha demostrat en estudis in vivo i in vitro. En alguns casos s'ha administrat una immunoteràpia passiva amb sèrum hiperimmune.[47] El tractament amb repel·lents de paparres resulta efectiu per a reduir les infestacions dels animals per paparres.[48]
Des de fa anys es treballa en el desenvolupament d'una vacuna contra aquest virus. A la dècada de 1970, el govern soviètic va aprovar l'ús d'una vacuna dissenyada a Bulgària, destinada a militars i treballadors destinats a zones de risc. Aquest i altres intents d'aconseguir una vacuna eficaç demostraren no ser viables pels efectes tòxics concomitants.[49] S'ha creat una vacuna emprant la Vacuna Ankara modificada (o Modified Vaccinia Ankara -MVA-) com a vector (és una vacuna atenuada basada en un poxvirus) que sembla donar una bona protecció en models murins. Ara bé, es considera que la manca d'animals de laboratori amb un sistema immunològic idoni limita molt aquest tipus de recerques.[50] Altres estudis indiquen que una MVA modificada que expressa una glicoproteïna determinada (MVA-GP) indueix la resposta immunitària cel·lular i humoral, un fet necessari per a poder assolir la protecció desitjada.[51]
Epidemiologia
modificaManteniment i transmissió
modificaEl VFHCC es manté a través de transmissió vertical i horitzontal mitjançant diversos gèneres de paparra de la família Ixodidae, també anomenades paparres dures. Aquestes transmeten el virus a una gran varietat de mamífers tant salvatges com domèstics, que desenvoluparan una virèmia transitòria (d'uns 2-15 dies) asimptomàtica. Les paparres, per això, romandran infectades permanentment, sent els reservoris principals de la malaltia. A Europa, el reservori prevalent és Hyalomma marginatum, si bé a la península ibèrica s'ha demostrat la presència del virus a exemplars de l'espècie Hyalomma lusitanicum, abundant al centre i sud-est. Quan les paparres ingereixen sang infectada, el VFHCC evita la seva resposta immune cel·lular i humoral i es replica al tracte digestiu. Després es dissemina per l'hemolimfa i infecta diferents teixits de la paparra, en especial les glàndules salivals i el sistema reproductiu. Aquestes interaccions virus-hoste són fonamentals per entendre els mecanismes de transmissió del VFHCC.[52]
Les persones també es veuen afectades, i la seva infecció si que és simptomàtica. La gran majoria de casos s'han donat en treballadors de la indústria ramadera, així com pastors, treballadors d'escorxador, veterinaris i personal sanitari en contacte amb líquids corporals de malalts infectats.[53]
Transmissió vertical
modificaEl VFHCC es transmet de manera transestadial, transovàrica i venèria en paparres dels gèneres Haemaphysalis i Hyalomma. Sabent que una femella és capaç de produir milers d'ous, podem deduir que fins i tot una ràtio baixa de transmissió transovàrica donarà lloc a una població considerable de paparres infectades. Les evidències d'aquesta forma de transmissió en paparres del gènere Amblyomma no són concloents.[54]
Transmissió horitzontal
modificaEl VFHCC es transmet de manera horitzontal directa, a través de les diverses fonts no vectorials del virus (vegeu Fonts); i de manera indirecta, a través de paparres de la família Ixodidae.
S'ha demostrat l'existència de 31 espècies diferents de paparres dures portadores d'aquest virus, incloses en els gèneres Haemaphysalis i Hyalomma.[55] Sent aquest últim el responsable de la transmissió del virus a persones. Es creu que Rhipicephalus bursa podria ser un vector eficaç del virus, sobre tot a les zones en les que és l'espècie predominant de paparra.[56]
El virus és transmés a través de les picades de les paparres, en les quals la saliva d'aquestes entra en contacte amb el torrent sanguini. Després de la picada, una paparra pot mantenir-se enganxada a l'animal durant setmanes, incrementant el risc de transmissió de la malaltia. A partir d'aquesta informació, sabem que la disseminació de la FHCC es dona principalment en els mesos de primavera i estiu, quan les paparres estan més actives.[57]
Fonts
modificaA més a més de l'ús de vectors, el VFHCC es transmet a través de sang, secrecions, òrgans o altres líquids corporals d'animals i persones infectats.[58] Això fa possible que es donin casos d'infecció nosocomial, deguts a l'esterilització incompetent de material mèdic o la contaminació d'aquest, així com la reutilització d'agulles.[59] El VFHCC s'inactiva totalment en els objectes contaminats emprant solucions desinfectants amb un 2% de glutaraldehid i un 1% d'hipoclorit, escalfades 30 minuts a 56 °C.[60] Com altres virus causants de febres hemorràgiques (Ebola, Marburg o Lassa, per exemple), el VFHCC és potencialment transmissible per via sexual.[61][62]
Prevenció i control
modificaEn llocs d'alta prevalença de FHCC, regulacions requereixen mesures preventives anti-paparres priori al transport de bestiar o trasllat d'aquest a l'escorxador, així com l'ús d'acaricides. També és recomanable prendre les mesures següents de prevenció per tal de reduir l'exposició al virus:[63]
- Portar vestimenta de protecció (mànigues llargues, pantalons llargs), així com guants.
- Portar vestimenta de colors clars per facilitar la detecció de paparres a la roba.
- Fer servir repel·lents aprovats a la roba i pell.
- Examinar de manera regular la roba i pell en busca de paparres. En cas de trobar-ne, eliminar-les de manera segura.
- Evitar àrees on les paparres són abundants i temporades en les que són més actives.
- Implementar una quarantena en els animals abans del trasllat a l'escorxadors.
- Fer servir pesticides de manera rutinària en els animals dues setmanes priori al sacrifici.
Vacunació
modificaActualment no hi ha cap vacuna disponible per persones o animals. Tot i així, s'han desenvolupat preparacions antigèniques inactivades a Bulgària. La seva eficàcia no ha estat demostrada.[64]
Una vacuna desenvolupada per un equip de recerca de la universitat d'Erciyes sembla haver desenvolupat una vacuna preventiva de la FHCC, que està pendent d'aprovació de la FDA.[65] Es treballa en una vacuna recombinant basada en el vector viral MVA (en anglès: Modified Vaccinia Ankara),[66] capaç d'activar el sistema immunològic, sense -a hores d'ara- aconseguir una protecció suficient.[67]
Impactes associats a la malaltia
modificaImpacte econòmic
modificaL'impacte econòmic derivat de la FHCC depèn fonamentalment de les mesures de control aplicades un cop se'n detecta un brot, ja que és una malaltia que afecta els humans però no és patògena pels seus hostes amplificadors, que són petits i grans remugants, principalment.
Les principals mesures de control que es consideren a l'hora de valorar les possibles pèrdues econòmiques són: control de colònies de paparres (vectors), control de poblacions d'animals salvatges que poden transmetre la malaltia (com ara porcs senglars), restricció de productes procedents de granges infectades, tancament i/o quarantena de granges infectades.[68]
L'impacte econòmic generat pel control de colònies de vectors és un dels més significatius, ja que les paparres són una de les principals vies de transmissió del VFHCC dels animals als humans i per tant, les inversions dedicades a tècniques de desinfecció i compra d'acaricides per la seva eliminació seran importants. D'altra banda, també cal tenir en compte que les paparres, a més de generar pèrdues econòmiques com a vectors i reservoris de la malaltia, també provoquen pèrdua de pes en els animals, anèmia i en malmeten la pell.
D'altra banda, les conseqüències econòmiques associades a la sanitat animal no són tant importants perquè aquesta és una malaltia que no manifesta símptomes en els animals infectats. No obstant, cal tenir en compte que després de la detecció d'un brot de FHCC en bestiar, ràpidament es prenen les mesures de control necessàries i de restricció en el transport i comerç de productes i animals infectats, fet que sí que comportarà pèrdues econòmiques importants a nivell de les granges infectades.
A més, com que la transmissió de la malaltia es produeix també per contacte directe amb teixits i líquids corporals d'animals infectats, no només a través de vectors, caldrà incrementar les precaucions en els escorxadors per tal d'evitar que els treballadors s'infectin, i aquestes mesures de seguretat extres augmentaran l'impacte econòmic de la malaltia.
En definitiva, l'impacte econòmic derivat de l'aparició de brots de FHCC s'origina a partir de l'aplicació de les mesures de control necessàries per evitar la difusió de la malaltia i assegurar-ne l'erradicació.
Impacte sanitari
modificaEls brots humans poden ser greus i de fet es consideren una amenaça important pels serveis de salut pública, degut al potencial epidèmic de la malaltia, l'elevada taxa de mortalitat que presenta (al voltant del 30%), el risc d'infecció nosocomial (hospitalària) i les dificultats que representen el tractament i la prevenció de la malaltia.[69] La infecció pel VFHCC en dones embarassades no és freqüent, però implica un alt risc de mort materna i fetal, a banda del perill de la seva extensió intrahospitalària.[70] A determinats països, com el Pakistan, el VFHCC es considera un virus en expansió[71] i s'han relacionat brots importants d'aquesta febre hemorràgica amb moviments de bestiar sense control sanitari, propis d'algunes celebracions tradicionals.[72]
La població que presenta major risc d'infecció pel és aquella que està directament vinculada al bestiar, com són els grangers, veterinaris i treballadors dels escorxadors, ja que són els que entren en contacte amb possibles animals infectats, líquids corporals i teixits contaminats d'aquests, picades de paparres dels mateixos animals... També serà susceptible a contagiar-se de la malaltia qualsevol que entri en contacte amb animals salvatges que puguin estar infectats o bé entrin en zones on és possible trobar paparres en abundància. Inclouríem dins aquests segon col·lectiu caçadors i excursionistes, per exemple.
En relació a l'impacte sanitari, també cal considerar el tipus d'explotació ramadera on es detecta el brot infecciós. En les explotacions intensives, tenim un major contacte entre humans i bestiar, però en canvi no és molt freqüent la presència de paparres. En les explotacions extensives, en canvi, el contacte entre humans i animals es redueix, però els animals tenen moltes més probabilitats de ser picats per paparres, vectors del VFHCC, ja que els espais verds són òptims pel desenvolupament de les poblacions d'aquests àcars i els seus estadis de nimfa. Així doncs, la persistència de les infeccions i casos humans són més comuns en les explotacions extensives.
Referències
modifica- ↑ Faye O, Fontenille D, Thonnon J, Gonzalez JP, et al «Transmission expérimentale du virus de la fièvre hémorragique de Crimée-Congo par la tique Rhipicephalus evertsi evertsi (Acarina: Ixodidae)» (en francès). Bull Soc Pathol Exot, 1999 Jul; 92 (3), pp: 143-147. Arxivat de l'original el 27 de juliol 2017. ISSN: 0037-9085. PMID: 10472436 [Consulta: 19 juliol 2017]. Arxivat 27 de juliol 2017 a Wayback Machine.
- ↑ Bażanów BA, Pacoń J, Gadzała Ł, Frącka A, et al «Vector and Serologic Survey for Crimean-Congo Hemorrhagic Fever Virus in Poland» (en anglès). Vector Borne Zoonotic Dis, 2017 Jul; 17 (7), pp: 510-513. DOI: 10.1089/vbz.2016.2075. PMID: 28514225 [Consulta: 19 juliol 2017].
- ↑ Spengler, JR; Bergeron, É; Rollin, PE «Seroepidemiological Studies of Crimean-Congo Hemorrhagic Fever Virus in Domestic and Wild Animals» (en anglès). PLoS Negl Trop Dis, 2016 Gen 7; 10 (1), pp: e0004210. DOI: 10.1371/journal.pntd.0004210. PMC: 4704823. PMID: 26741652 [Consulta: 15 abril 2017].
- ↑ «OMS - Fiebre hemorrágica de Crimea-Congo» (en castellà), 01-01-2013. [Consulta: 10 gener 2016].
- ↑ Lukashev, AN; Klimentov, AS; Smirnova, SE; Dzagurova, TK; et al «Phylogeography of Crimean Congo Hemorrhagic Fever Virus» (en anglès). PLoS One, 2016 Nov 23; 11 (11), pp: e0166744. DOI: 10.1371/journal.pone.0166744. PMID: 27880794 [Consulta: 13 desembre 2016].
- ↑ Wiktorowicz, CJ; Arnold, B; Wiktorowicz, JE; Murray, ML; Kurosky, A «Hemorrhagic fever virus, human blood, and tissues in Iron Age mortuary vessels» (en anglès). Journal of Archaeological Science, 2017 Feb; 78, pp: 29-39. DOI: 10.1016/j.jas.2016.11.009 [Consulta: 15 desembre 2016].
- ↑ «Informe de situación. Riesgo de FHCC en España» (en castellà). Arxivat de l'original el 2018-04-29. [Consulta: 10 gener 2016].
- ↑ «Fiebre hemorrágica de Crimea-Congo» (en castellà). Center for Food Security & Public Health, Institute for International Cooperation in Animal Biologics, 01-10-2009. Arxivat de l'original el 2016-09-10. [Consulta: 10 gener 2016].
- ↑ 9,0 9,1 Hoogstraal, H. «The epidemiology of tick-borne Crimean–Congo hemorrhagic fever in Asia, Europe, and Africa». J. Med. Entomol., 15, 1979.
- ↑ Chumakov, M.P. A new tick-borne virus disease—Crimean hemorrhagic fever, 1944.
- ↑ Casals, J. Antigenic similarity between the virus causing Crimean hemorrhagic fever and Congo virus, 1969.
- ↑ Chumakov, MP; Smirnova, SE; Tkachenko, EA «Relationship between strains of Crimean haemorrhagic fever and Congo viruses» (en anglès). Acta Virol, 1970 Jan; 14 (1), pp: 82-85. PMID: 4392083 [Consulta: 12 desembre 2016].
- ↑ Papa A, Dalla V, Papadimitriou E, Kartalis GN, Antoniadis A «Emergence of Crimean–Congo haemorrhagic fever in Greece» (en anglès). Clin Microbiol Infect, 2010 Jul; 16 (7), pp: 843-847. DOI: 10.1111/j.1469-0691.2009.02996.x. PMID: 19845692 [Consulta: 10 juliol 2017].[Enllaç no actiu]
- ↑ Estrada-Peña, A; Palomar, AM; Santibáñez, P; et al «Crimean-Congo hemorrhagic fever virus in ticks, Southwestern Europe, 2010» (en anglès). Emerg Infect Dis, 2012 Jan; 18 (1), pp. 179-80. DOI: 10.3201/eid1801.111040. PMID: 22261502 [Consulta: 7 agost 2016].
- ↑ Palomar, AM; Portillo, A; Santibáñez, P; et al «Crimean-Congo Hemorrhagic Fever Virus in Ticks from Migratory Birds, Morocco» (en anglès). Emerg Infect Dis, 2013 Feb; 19 (2), pp. 260-3. DOI: 10.3201/eid1902.121193. PMID: 23347801 [Consulta: 7 agost 2016].
- ↑ Berwick, Angus «First Local Case of Tick-Borne Disease Kills Man in Spain». Scientific American. Public Health, 03-09-2016 [Consulta: 4 setembre 2016].
- ↑ Sánchez Ugart, Daniel «Confirmats els dos primers casos de febre hemorràgica Crimea-Congo a Espanya». ara.cat, 01-09-2016 [Consulta: 2 setembre 2016].
- ↑ Red Nacional de Vigilancia Epidemiológica «Protocolo de Vigilancia de la Fiebre Hemorrágica por virus Crimea-Congo» (en castellà). Vigilancia epidemiològica, Ministerio de Sanidad, Servicios Sociales e Igualdad, 2016, Sep, pàg. 232. Arxivat de l'original el 20 de desembre 2016 [Consulta: 12 desembre 2016].
- ↑ Pieck, Karla Islas «Los casos autóctonos de fiebre hemorrágica de Crimea-Congo implicarán cambios en los protocolos europeos» (en castellà). Medscape. Noticias y Perspectivas, 09-09-2016 [Consulta: 11 setembre 2016].
- ↑ Palomar, AM; Portillo, A; Santibáñez, S; García-Álvarez, L; et al «Molecular (ticks) and serological (humans) study of Crimean-Congo hemorrhagic fever virus in the Iberian Peninsula, 2013-2015» (en anglès/castellà). Enferm Infecc Microbiol Clin, 2017; Mar 10, pii: S0213-005X(17)30061-7. Arxivat de l'original el 2 d’abril 2017. DOI: 10.1016/j.eimc.2017.01.009. PMID: 28291670 [Consulta: 1r abril 2017]. Arxivat 2 April 2017[Date mismatch] a Wayback Machine.
- ↑ Ministerio de Sanidad, Servicios Sociales e Igualdad «Informe de situación y evaluación del riesgo de transmisión de Fiebre Hemorrágica de Crimea-Congo (FHCC) en España» (en castellà). Salud pública. Información sobre enfermedades emergentes. Enfermedad hemorrágica por virus Crimea-Congo, 2017; Abr 11, pàgs: 32. Arxivat de l'original el 26 d’abril 2017 [Consulta: 25 abril 2017].
- ↑ Negredo, A; de la Calle‑Prieto, F; Palencia-Herrejón, E; Mora-Rillo, M; et al «Autochthonous Crimean–Congo Hemorrhagic Fever in Spain» (en anglès). N Engl J Med, 2017 Jul 13; 377, pp: 154-161. DOI: 10.1056/NEJMoa1615162 [Consulta: 13 juliol 2017].
- ↑ Al-Abri, SS; Abaidani, IA; Fazlalipour, M; Mostafavi, E; et al «Current status of Crimean-Congo haemorrhagic fever in the World Health Organization Eastern Mediterranean Region: issues, challenges, and future directions» (en anglès). Int J Infect Dis, 2017 Mar 1; 58, pp: 82-89. DOI: 10.1016/j.ijid.2017.02.018. PMID: 28259724 [Consulta: 15 abril 2017].
- ↑ Leblebicioglu H, Eroglu C, Erciyas-Yavuz K, Hokelek M, et al «Role of migratory birds in spreading Crimean-Congo hemorrhagic fever, Turkey» (en anglès). Emerg Infect Dis, 2014 Ag; 20 (8), pp: 1331-1334. DOI: 10.3201/eid2008.131547. PMC: 4111188. PMID: 25062428 [Consulta: 30 maig 2017].
- ↑ WHO «2017 Annual review of diseases prioritized under the Research and Development Blueprint» (en anglès). WHO Research and Development Blueprint, 2017, 24-25 Gen, pàgs: 16 [Consulta: 28 juliol 2017].
- ↑ Fauqet. Virus Taxonomy:Eighth Report of the International Committee on Taxonomy of Viruses. San Diego, Calif.: Elsevier Academic Press,, 2005.
- ↑ R. Flick, C.A. Whitehouse «Crimean–Congo hemorrhagic fever virus». Current Molecular Medicine, 2005.
- ↑ Deyde, VM; Khristova, ML; Rollin, PE; Ksiazek, TG; Nichol, ST «Crimean-Congo hemorrhagic fever virus genomics and global diver» (en anglès). J Virol, 2006 Sep; 80 (17), pp: 8834-8842. DOI: 10.1128/JVI.00752-06. PMC: 1563879. PMID: 16912331 [Consulta: 25 abril 2017].
- ↑ Dennis A. Bente, Naomi L. Forrester, Douglas M. Watts, Alexander J. McAuley, Chris A. Whitehouse, Mike Bray «Crimean-Congo hemorrhagic fever: History, epidemiology, pathogenesis, clinical syndrome and genetic diversity». Antiviral Research, Volume 64, Issue 3, 2004.
- ↑ Whitehouse, C. «Crimean–Congo hemorrhagic fever». Science Direct, 2004.
- ↑ Carroll SA, Bird BH, Rollin PE, Nichol ST «Ancient common ancestry of Crimean-Congo hemorrhagic fever virus». Mol Phylogenet Evol, 2010.
- ↑ 32,0 32,1 Whitehouse, C.A: «Crimean–Congo Hemorrhagic Fever Virus and Other Nairoviruses». Encyclopedia of Virology, Science Direct, 2008.
- ↑ Xia, H; Beck, AS; Gargili, A; Forrester, N; et al «Transstadial Transmission and Long-term Association of Crimean-Congo Hemorrhagic Fever Virus in Ticks Shapes Genome Plasticity» (en anglès). Sci Rep, 2016 Oct 24; 6, pp: 35819. DOI: 10.1038/srep35819. PMC: 5075774. PMID: 27775001 [Consulta: 15 desembre 2016].
- ↑ Sherifi K, Cadar D, Muji S, Robaj A, et al «Crimean-Congo hemorrhagic fever virus clades V and VI (Europe 1 and 2) in ticks in Kosovo, 2012» (en anglès). PLoS Negl Trop Dis, 2014 Sep 25; 8 (9), pp: e3168. DOI: 10.1371/journal.pntd.0003168. PMC: 4177860. PMID: 25255381 [Consulta: 10 juliol 2017].
- ↑ Papa, A; Mirazimi, A; Köksal, I; Estrada-Pena, A; Feldmann, H «Recent advances in research on Crimean-Congo hemorrhagic fever» (en anglès). J Clin Virol, 2015 Mar; 64, pp: 137-143. DOI: 10.1016/j.jcv.2014.08.029. PMC: 4346445. PMID: 25453328 [Consulta: 24 abril 2017].
- ↑ Lindeborg, M; Barboutis, C; Ehrenborg, C; et al «Migratory birds, ticks, and crimean-congo hemorrhagic fever virus» (en anglès). Emerg Infect Dis, 2012 Dec; 18 (12), pp. 2095-7. DOI: 10.3201/eid1812.120718. PMID: 23171591 [Consulta: 7 agost 2016].
- ↑ Yashina, L; Vyshemirskii, O; Seregin, S; Petrova, I; et al «Genetic analysis of Crimean-Congo hemorrhagic fever virus in Russia» (en anglès). J Clin Microbiol, 2003 Feb; 41 (2), pp: 860-862. PMC: 149693. PMID: 12574301 [Consulta: 16 abril 2017].
- ↑ Oany, AR; Ahmad, SA; Hossain, MU; Jyoti, TP «Identification of highly conserved regions in L-segment of Crimean-Congo hemorrhagic fever virus and immunoinformatic prediction about potential novel vaccine» (en anglès). Adv Appl Bioinform Chem, 2015 Jan 8; 8, pp: 1-10. DOI: 10.2147/AABC.S75250. PMC: 4293217. PMID: 25609983 [Consulta: 15 desembre 2016].
- ↑ 39,0 39,1 39,2 «OMS Fiebre hemorrágica de Crimea Congo» (en castellà). Centro de prensa OMS, Enero 2013. [Consulta: 9 gener 2016].
- ↑ 40,0 40,1 «Fiebre hemorrágica de Crimea Congo» (en castellà). Iowa State University College of Veterinary Medicine, 01-10-2009. [Consulta: 9 gener 2016].
- ↑ Aktaş, T; Aktaş, F; Özmen, Z; Altunkaş, A; et al «Thorax CT findings in patients with Crimean-Congo hemorrhagic fever (CCHF)» (en anglès). Springerplus, 2016 Oct 21; 5(1), pp: 1823. DOI: 10.1186/s40064-016-3522-5. PMC: 5074938. PMID: 27818861 [Consulta: 20 desembre 2016].
- ↑ Büyüktuna, SA; Doğan, HO; Bakır, D; Erşan, S; et al «Increased irisin concentrations in patients with Crimean-Congo hemorràgic fever» (en anglès). Jpn J Infect Dis, 2017 Feb 28, pàgs: 15. DOI: 10.7883/yoken.JJID.2016.432. PMID: 28250262 [Consulta: 15 abril 2017].
- ↑ Pshenichnaya, NY; Sannikova, IV «Probable Crimean-Congo hemorrhagic fever virus transmission occurred after aerosol-generating medical procedures in Russia: nosocomial cluster» (en anglès). Int J Infect Dis, 2015 Abr; 33, pp: 120-122. DOI: 10.1016/j.ijid.2014.12.047. PMID: 25576827 [Consulta: 15 abril 2017].
- ↑ «Fiebre Hemorrágica de Crimea-Congo». The Center for Food Security and Public Health, 2009, pàg. 2. Arxivat de l'original el 2016-07-01 [Consulta: 30 desembre 2015]. Arxivat 2016-09-10 a Wayback Machine.
- ↑ «Informe de situación y evaluación del riesgo de transmisión de la Fiebre Hemorrágica de Crimea-Congo en España». Ministerio de sanidad, política social e igualdad, 10-2011, pàg. 21. Arxivat de l'original el 2016-09-08 [Consulta: 30 desembre 2015].
- ↑ Oestereich, L; Rieger, T; Neumann, M; Bernreuther, C; et al «Evaluation of antiviral efficacy of ribavirin, arbidol, and T-705 (favipiravir) in a mouse model for Crimean-Congo hemorrhagic fever» (en anglès). PLoS Negl Trop Dis, 2014 May 1; 8 (5), pp: e2804. DOI: 10.1371/journal.pntd.0002804. PMC: 4006714. PMID: 24786461 [Consulta: 20 desembre 2016].
- ↑ Kubar, A; Haciomeroglu, M; Ozkul, A; Bagriacik, U; et al «Prompt administration of Crimean-Congo hemorrhagic fever (CCHF) virus hyperimmunoglobulin in patients diagnosed with CCHF and viral load monitorization by reverse transcriptase-PCR» (en anglès). Jpn J Infect Dis, 2011; 64 (5), pp: 439-443. Arxivat de l'original el 23 de desembre 2016. PMID: 21937830 [Consulta: 21 desembre 2016]. Arxivat 23 de desembre 2016 a Wayback Machine.
- ↑ «Fiebre hemorrágica de Crimea-Congo». Manual Terrestre de la OIE 2014, Capítulo 2.1.3b., 2014, pàg. 1.[Enllaç no actiu]
- ↑ Papa, A; Mirazimi, A; Köksal, I; Estrada-Pena, A; Feldmann, H «Recent advances in research on Crimean-Congo hemorrhagic fever» (en anglès). J Clin Virol, 2015 Mar; 64, pp: 137-143. DOI: 10.1016/j.jcv.2014.08.029. PMC: 4346445. PMID: 25453328 [Consulta: 25 març 2017].
- ↑ Buttigieg, KR; Dowall, SD; Findlay-Wilson, S; Miloszewska, A; et al «A Novel Vaccine against Crimean-Congo Haemorrhagic Fever Protects 100% of Animals against Lethal Challenge in a Mouse Model» (en anglès). PLoS One, 2014 Mar 12; 9 (3), pp: e91516. DOI: 10.1371/journal.pone.0091516. PMC: 3951450. PMID: 24621656 [Consulta: 25 març 2017].
- ↑ Dowall, SD; Graham, VA; Rayner, E; Hunter, L; et al «Protective effects of a Modified Vaccinia Ankara-based vaccine candidate against Crimean-Congo Haemorrhagic Fever virus require both cellular and humoral responses» (en anglès). PLoS One, 2016 Jun 7; 11 (6), pp: e0156637. DOI: 10.1371/journal.pone.0156637. PMC: 4896484. PMID: 27272940 [Consulta: 25 març 2017].
- ↑ Papa A, Tsergouli K, Tsioka K, Mirazimi A «Crimean-Congo Hemorrhagic Fever: Tick-Host-Virus Interactions» (en anglès). Front Cell Infect Microbiol, 2017 Maig 26; 7, pp: 213. DOI: 10.3389/fcimb.2017.00213. PMC: 5445422. PMID: 28603698 [Consulta: 19 juliol 2017].
- ↑ Bente DA, Forrester NL, Watts DM, McAuley AJ, et al «Crimean-Congo hemorrhagic fever: History, epidemiology, pathogenesis, clinical syndrome and genetic diversity» (en anglès). Antiviral Res, 2013 Oct; 100 (1), pp: 159-189. DOI: 10.1016/j.antiviral.2013.07.006. PMID: 23906741 [Consulta: 20 juliol 2017].
- ↑ Faye, O; Cornet, JP; Camicas, JL; Fontenille, D; Gonzalez, JP «Transmission expérimentale du virus de la fièvre hémorragique de Crimée-Congo: place de trois espèces vectrices dans les cycles de maintenance et de transmission au Sénégal» (en francès). Parasite, 1999 Mar; 6 (1), pp: 27-32. DOI: 10.1051/parasite/1999061027. PMID: 10229934 [Consulta: 14 abril 2017].
- ↑ Mehravaran A1, Moradi M, Telmadarraiy Z, Mostafavi E, et al. «Molecular detection of Crimean-Congo haemorrhagic fever (CCHF) virus in ticks from southeastern Iran» (en anglès). Ticks Tick Borne Dis, 2013 Feb; 4 (1-2), pp: 35-38. [Consulta: 10 juliol 2017].
- ↑ Tonbak S, Aktas M, Altay K, Azkur AK, et al «Crimean-Congo Hemorrhagic Fever Virus: Genetic Analysis and Tick Survey in Turkey» (en anglès). J Clin Microbiol, 2006 Nov; 44 (11), pp: 4120-4124. DOI: 10.1128/JCM.00644-06. PMC: 1698322. PMID: 17088370 [Consulta: 10 juliol 2017].
- ↑ Estrada-Peña, A; Ruiz-Fons, F; Acevedo, P; Gortazar, C; de la Fuente, J «Factors driving the circulation and possible expansion of Crimean-Congo haemorrhagic fever virus in the western Palearctic» (en anglès). J Appl Microbiol, 2013 Gen; 114 (1), pp: 278-286. DOI: 10.1111/jam.12039. PMID: 23061817 [Consulta: 14 abril 2017].
- ↑ Pshenichnaya, NY; Nenadskaya, SA «Probable Crimean-Congo hemorrhagic fever virus transmission occurred after aerosol-generating medical procedures in Russia: nosocomial cluster» (en anglès). Int J Infect Dis, 2015 Abr; 33, pp: 120-122. DOI: 10.1016/j.ijid.2014.12.047. PMID: 25576827 [Consulta: 14 abril 2017].
- ↑ Naderi, HR; Sheybani, F; Bojdi, A; Khosravi, N; Mostafavi, I «Fatal nosocomial spread of Crimean-Congo hemorrhagic fever with very short incubation period» (en anglès). Am J Trop Med Hyg, 2013 Mar; 88 (3), pp: 469-471. DOI: 10.4269/ajtmh.2012.12-0337. PMC: 3592527. PMID: 23269658 [Consulta: 14 abril 2017].
- ↑ Aslam, S; Latif, MS; Daud, M; Rahman, ZU; et al «Crimean-Congo hemorrhagic fever: Risk factors and control measures for the infection abatement» (en anglès). Biomed Rep, 2016 Gen; 4 (1), pp: 15-20. DOI: 10.3892/br.2015.545. PMC: 4726894. PMID: 26870327 [Consulta: 24 abril 2017].
- ↑ Ergonul, O; Battal, I «Potential sexual transmission of Crimean-Congo hemorrhagic fever infection» (en anglès). Jpn J Infect Dis, 2014; 67 (2), pp: 137-138. PMID: 24647261 [Consulta: 14 abril 2017].
- ↑ Pshenichnaya, NY; Sydenko, IS; Klinovaya, EP; Romanova, EB; Zhuravlev, AS «Possible sexual transmission of Crimean-Congo hemorrhagic fever» (en anglès). Int J Infect Dis, 2016 Abr; 45, pp: 109-111. DOI: 10.1016/j.ijid.2016.02.1008. PMID: 26972040 [Consulta: 14 abril 2017].
- ↑ «Crimean-Congo haemorrhagic fever».
- ↑ «Crimean-Congo hemorrhagic fever: Current and future prospects of vaccines and therapies ☆».
- ↑ «Tick vaccine gospel Crimean-Congo Hemorrhagic Fever (CCHF) for the development of vaccines against the disease, the study carried out by Turkish scientists received positive results.».
- ↑ Dowall, SD; Graham, VA; Rayner, E; Hunter, L; et al «Protective effects of a Modified Vaccinia Ankara-based vaccine candidate against Crimean-Congo Haemorrhagic Fever virus require both cellular and humoral responses» (en anglès). PLoS One, 2016 Jun 7; 11 (6), pp. e0156637. DOI: 10.1371/journal.pone.0156637. PMID: 27272940 [Consulta: 8 setembre 2016].
- ↑ Dowall, SD; Buttigieg, KR; Findlay-Wilson, SJ; Rayner, E; et al «A Crimean-Congo hemorrhagic fever (CCHF) viral vaccine expressing nucleoprotein is immunogenic but fails to confer protection against lethal disease» (en anglès). Hum Vaccin Immunother, 2016 Aug 26; 12 (2), pp. 519-27. DOI: 10.1080/21645515.2015.1078045. PMID: 26309231 [Consulta: 8 setembre 2016].
- ↑ «Risk Assessment of Crimean Congo Haemorrhagic Fever in Western Europe» (en anglès). Central Veterinary Institute of Wageningen University & Research, 2012. [Consulta: 3 gener 2016].
- ↑ «La fiebre hemorrágica de Crimea-Congo, las infecciones por hantavirus y la fiebre hemorrágica de Alkhurma, enfermedades infecciosas emergentes» (en castellà). OMS. Consell executiu, 127, 2010. [Consulta: 3 gener 2016].
- ↑ Pshenichnaya, NY; Leblebicioglu, H; Bozkurt, I; Sannikova, IV; et al «Crimean-Congo hemorrhagic fever in pregnancy: A systematic review and case series from Russia, Kazakhstan and Turkey» (en anglès). Int J Infect Dis, 2017 Feb 26, pii: S1201-9712(17)30066-8. DOI: 10.1016/j.ijid.2017.02.019. PMID: 28249811 [Consulta: 24 març 2017].
- ↑ Qidwai, W «Crimean-Congo Haemorrhagic Fever: An Emerging Public Health Care Challenge in Pakistan» (en anglès). J Coll Physicians Surg Pak, 2016 Feb; 26 (2), pp: 81-82. DOI: 02.2016/JCPSP.8182. PMID: 26876389 [Consulta: 4 maig 2017].
- ↑ Karim, AM; Hussain, I; Lee, JH; Park, KS; Lee, SH «Surveillance of Crimean-Congo haemorrhagic fever in Pakistan» (en anglès). Lancet Infect Dis, 2017 Abr; 17 (4), pp: 367-368. DOI: 10.1016/S1473-3099(17)30119-6. PMID: 28346174 [Consulta: 4 maig 2017].
Enllaços externs
modifica- «Febre hemorràgica de Crimea-Congo». Canal Salut. Generalitat de Catalunya.
- «Febre hemorràgica de Crimea-Congo». Departament de Salut. Generalitat de Catalunya. Arxivat de l'original el 2016-09-16. [Consulta: 16 setembre 2016].
- «Protocol d'actuació davant casos sospitosos de febre hemorràgica de Crimea-Congo». Secretaria de Salut Pública. Departament de Salut. Generalitat de Catalunya, actualització: 2/10/2016. Arxivat de l'original el 2016-09-16. [Consulta: 12 desembre 2016].
- «Crimean Congo Haemorrhagic Fever». Zulfiquar, A (en anglès). [Consulta: 16 setembre 2016].